Đề kiểm tra giữa học kì I môn : Hóa 10 ; đề 1 ( thời gian làm bài 45 phút)
Bạn đang xem tài liệu "Đề kiểm tra giữa học kì I môn : Hóa 10 ; đề 1 ( thời gian làm bài 45 phút)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
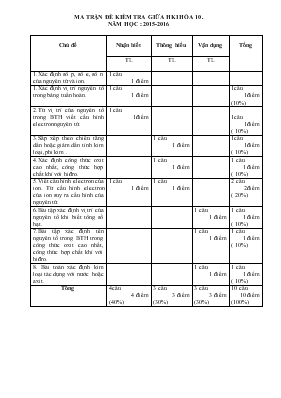
MA TRẬN ĐỀ KIỂM TRA GIỮA HKI HÓA 10 . NĂM HỌC : 2015-2016 Chủ đề Nhận biết Thông hiểu Vận dụng Tổng TL TL TL 1.Xác định số p, số e, số n của nguyên tử và ion. 1 câu 1 điểm 1.Xác định vị trí nguyên tố trong bảng tuần hoàn. 1 câu 1 điểm 1câu 1điểm (10%) 2.Từ vị trí của nguyên tố trong BTH viết cấu hình electron nguyên tử. 1 câu 1điểm 1câu 1điểm ( 10%) 3.Sắp xếp theo chiều tăng dần hoặc giảm dần tính kim loại, phi kim . 1 câu 1 điểm 1câu 1điểm ( 10%) 4.Xác định công thức oxit cao nhất, công thức hợp chất khí với hiđro. 1 câu 1 điểm 1 câu 1 điểm ( 10%) 5.Viết cấu hình electron của ion. Từ cấu hình electron của ion suy ra cấu hình của nguyên tử. 1 câu 1 điểm 1 câu 1 điểm 2 câu 2điểm ( 20%) 6.Bài tập xác định vị trí của nguyên tố khi biết tổng số hạt. 1 câu 1 điểm 1 câu 1 điểm ( 10%) 7.Bài tập xác định tên nguyên tố trong BTH trong công thức oxit cao nhất, công thức hợp chất khí với hiđro. 1 câu 1 điểm 1 câu 1 điểm ( 10%) 8. Bài toán xác định kim loại tác dụng với nước hoặc axit. 1 câu 1 điểm 1 câu 1 điểm ( 10%) Tổng 4câu 4 điểm (40%) 3 câu 3 điểm (30%) 3 câu 3 điểm (30%) 10 câu 10 điểm (100%) ĐỀ KIỂM TRA GIỮA HKI MÔN : HÓA 10 ; Đề 1 ( Thời gian làm bài 45 phút) Câu 1: Xác định số proton, nơtron, electron trong các nguyên tử và ion sau: a) b) Câu 2: Viết cấu hình electron nguyên tử và xác định vị trí của các nguyên tố sau trong bảng tuần hoàn ( 1 điểm) a) Na ( Z = 11) b) P ( Z = 15) Câu 3: Viết cấu hình electron nguyên tử của nguyên tố X thuộc chu kì 3, nhóm IIA. ( 1 điểm) Câu 4: Cho các nguyên tố: K ( Z = 19); Mg (Z = 12); Al (Z = 13); Na (Z = 11). Sắp xếp các nguyên tố trên theo thứ tự tính kim loại giảm dần? ( 1 điểm) Câu 5: Nguyên tố R ở ô 16, nhóm VIA, chu kì 3. Viết công thức oxit cao nhất và công thức hợp chất khí với hiđro của R. ( 1 điểm) Câu 6: Viết cấu hình electron của các ion sau: ( 1 điểm) a) ion ( biết Cl có Z = 17) b) ion ( biết Ca có Z = 20) Câu 7: Anion có cấu hình electron .Viết cấu hình electron của nguyên tử X? ( 1 điểm) Câu 8: Nguyên tử của nguyên tố R có tổng số hạt proton, nơtron và electron là 54, trong đó số nơtron nhiều hơn số electron là 3 hạt.Tính số khối (A) của nguyên tử nguyên tố R. ( 1điểm) Câu 9: Oxit cao nhất của nguyên tố R là , trong hợp chất của nó với hiđro có 5,88 % H về khối lượng . Xác định nguyên tử khối của nguyên tố R. (Cho S = 32; Se = 79) ( 1 điểm) Câu 10: Cho 0,6 gam một kim loại M thuộc nhóm IIA tác dụng với nước thì có 0,336 lít khí thoát ra ( đktc) . Xác định kim loại M ? ( cho Be = 9; Mg = 12;Ca = 40; Ba = 137) ( 1 điểm) ( Học sinh không được sử dụng bảng hệ thống tuần hoàn) ĐỀ KIỂM TRA GIỮA HKI MÔN : HÓA 10; Đề 2: ( Thời gian làm bài 45 phút) Câu 1: Xác định số proton, nơtron, electron trong các nguyên tử và ion sau: a) b) Câu 2:Viết cấu hình electron nguyên tử và xác định vị trí của các nguyên tố sau trong bảng tuần hoàn ( 1 điểm) a) Mg ( Z = 12) b) Si ( Z = 14) Câu 3: Viết cấu hình electron nguyên tử nguyên tố Y thuộc chu kì 2, nhóm VIIA. ( 1điểm) Câu 4: Cho các nguyên tố: I ( Z = 53); Br ( Z = 35); F ( Z = 9); Cl ( Z = 17). Sắp xếp các nguyên tố trên theo thứ tự tính phi kim tăng dần? ( 1 điểm) Câu 5: Nguyên tố R ở ô 14, nhóm IVA, chu kì 3. Viết công thức oxit cao nhất và công thức hợp chất khí với hiđro của R. ( 1 điểm) Câu 6: Viết cấu hình electron của các ion sau: ( 1 điểm) a) ion ( biết S có Z = 16) b) ion ( biết K có Z = 19) Câu 7: Cation có cấu hình electron .Viết cấu hình electron của nguyên tử M? ( 1 điểm) Câu 8: Trong nguyên tử X tổng số hạt proton, nơtron, electron là 28. Biết rằng số nơtron bằng số proton cộng thêm 1 . Tìm số khối của nguyên tử X ? ( 1điểm) Câu 9: Oxit cao nhất của nguyên tố R có dạng . Hợp chất khí với hiđro của nguyên tố này chứa 8,82% H về khối lượng .Xác định nguyên tố R? (Cho N = 14; P = 31; As = 75) ( 1 điểm) Câu 10: Cho 0,69 gam một kim loại M nhóm IA tác dụng với nước (dư ) thu được 0,336 lít khí ( đktc) . Xác định kim loại kiềm M ? ( cho Li = 7; Na = 23; K = 39; Rb = 85; Cs = 133) ( 1 điểm) ( Học sinh không được sử dụng bảng hệ thống tuần hoàn) ĐÁP ÁN KIỂM TRA GIỮA HKI ; NĂM HỌC : 2015-2016 MÔN HOÁ 10; ĐỀ 1 NỘI DUNG ĐIỂM Câu 1: Xác định số proton, nơtron, electron trong các nguyên tử và ion sau: a) b) ĐÁP: số p = số e = 9; số n = 10 số p =13; số e = 10; số n = 14 0,5 0,5 Câu 2: Viết cấu hình electron nguyên tử và xác định vị trí của các nguyên tố sau trong bảng tuần hoàn ( 1 điểm) a) Na ( Z = 11) b) P ( Z = 15) ĐÁP: a) Na ( Z = 11) CH e: . Ô 11, chu kì 3; nhóm IA. b)P ( Z = 15) CH e: . Ô 15, chu kì 3; nhóm VA 0,5 0,5 Câu 3: Viết cấu hình electron nguyên tử của nguyên tố X thuộc chu kì 3, nhóm IIA. ( 1 điểm) ĐÁP: CH e: 1 Câu 4: Cho các nguyên tố: K ( Z = 19); Mg (Z = 12); Al (Z = 13); Na (Z = 11). Sắp xếp các nguyên tố trên theo thứ tự tính kim loại giảm dần? ( 1 điểm) ĐÁP: -Thứ tự tính kim loại giảm dần: K > Na > Mg > Al. 1 Câu 5: Nguyên tố R ở ô 16, nhóm VIA, chu kì 3. Viết công thức oxit cao nhất và công thức hợp chất khí với hiđro của R. ( 1 điểm) ĐÁP: Công thức oxit cao nhất: . Công thức hợp chất khí với hiđro: 0,5 0,5 Câu 6: Viết cấu hình electron của các ion sau: ( 1 điểm) a) ion ( biết Cl có Z = 17) b) ion ( biết Ca có Z = 20) ĐÁP: : : 0,5 0,5 Câu 7: Anion có cấu hình electron .Viết cấu hình electron của nguyên tử X? ( 1 điểm) ĐÁP: CH e : 1 Câu 8: Nguyên tử của nguyên tố R có tổng số hạt proton, nơtron và electron là 54, trong đó số nơtron nhiều hơn số electron là 3 hạt.Tính số khối (A) của nguyên tử nguyên tố R. ( 1điểm) ĐÁP: A= 17+ 20 =37 0,25 0,25 0,25 0,25 Câu 9: Oxit cao nhất của một nguyên tố là , trong hợp chất của nó với hiđro có 5,88 % H về khối lượng . Xác định nguyên tử khối của nguyên tố đó. (Cho S = 32; Se = 79) ( 1 điểm) ĐÁP: Oxit cao nhất của một nguyên tố là Hợp chất khí với hiđro của nguyên tố R là Vậy R là S 0,25 0,25 0,25 0,25 Câu 10: Cho 0,6 gam một kim loại M thuộc nhóm IIA tác dụng với nước thì có 0,336 lít khí thoát ra ( đktc) . Xác định kim loại M ? ( cho Be = 9; Mg = 12;Ca = 40; Ba = 137) ( 1 điểm) ĐÁP: Vậy M là Ca 0,25 0,25 0,25 0,25 ĐÁP ÁN KIỂM TRA GIỮA HKI ; NĂM HỌC : 2014-2015 MÔN HOÁ 10; ĐỀ 2 NỘI DUNG ĐIỂM Câu 1: Xác định số proton, nơtron, electron trong các nguyên tử và ion sau: a) b) ĐÁP: số p = số e = 18; số n = 22 số p =26; số e = 24; số n = 30 0,5 0,5 Câu 2:Viết cấu hình electron nguyên tử và xác định vị trí của các nguyên tố sau trong bảng tuần hoàn ( 1 điểm) a) Mg ( Z = 12) b) Si ( Z = 14) ĐÁP: a) Mg ( Z = 12) CH e: . Ô 12, chu kì 3; nhóm IIA. b)Si ( Z = 14) CH e: . Ô 14, chu kì 3; nhóm IVA 0,5 0,5 Câu 3: Viết cấu hình electron nguyên tử nguyên tố Y thuộc chu kì 2, nhóm VIIA. ( 1điểm) ĐÁP: CH e: 1 Câu 4: Cho các nguyên tố: I ( Z = 53); Br ( Z = 35); F ( Z = 9); Cl ( Z = 17). Sắp xếp các nguyên tố trên theo thứ tự tính phi kim tăng dần? ( 1 điểm) ĐÁP: -Thứ tự tính phi kim tăng dần: I < Br < Cl < F 1 Câu 5: Nguyên tố R ở ô 14, nhóm IVA, chu kì 3. Viết công thức oxit cao nhất và công thức hợp chất khí với hiđro của R. ( 1 điểm) ĐÁP: -Công thức oxit cao nhất: . -Công thức hợp chất khí với hiđro: 0,5 0,5 Câu 6: Viết cấu hình electron của các ion sau: ( 1 điểm) a) ion ( biết S có Z = 16) b) ion ( biết K có Z = 19) ĐÁP: : : 0,5 0,5 Câu 7: Cation có cấu hình electron .Viết cấu hình electron của nguyên tử M? ( 1 điểm) ĐÁP: CH e: 1 Câu 8: Trong nguyên tử X tổng số hạt proton, nơtron, electron là 28. Biết rằng số nơtron bằng số proton cộng thêm 1 . Tìm số khối của nguyên tử X ? ( 1điểm) ĐÁP: A= 9+10 = 19 0,25 0,25 0,25 0,25 Câu 9: Oxit cao nhất của một nguyên tố có dạng . Hợp chất khí với hiđro của nguyên tố này chứa 8,82% H về khối lượng .Xác định nguyên tố R?(Cho N = 14; P = 31; As = 75) ( 1 điểm) ĐÁP: Oxit cao nhất của R có công thức R thuộc nhóm VA. Công thức của R trong hợp chất với hiđro là : Vậy R là photpho ( P) 0,25 0,25 0,25 0,25 Câu 10: Cho 0,69 gam một kim loại M nhóm IA tác dụng với nước (dư ) thu được 0,336 lít khí ( đktc) . Xác định kim loại M ? ( cho Li = 7; Na = 23; K = 39; Rb = 85; Cs = 133) ( 1 điểm) ĐÁP: Vậy M là Natri (Na) 0,25 0,25 0,25 0,25
Tài liệu đính kèm:
 KT giua HKI Hoa 10 (Diep).doc
KT giua HKI Hoa 10 (Diep).doc





