Kiểm tra học kì 1 - Năm 2013 - 2014 môn hóa – Lớp 8 (thời gian làm bài 45 phút)
Bạn đang xem tài liệu "Kiểm tra học kì 1 - Năm 2013 - 2014 môn hóa – Lớp 8 (thời gian làm bài 45 phút)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
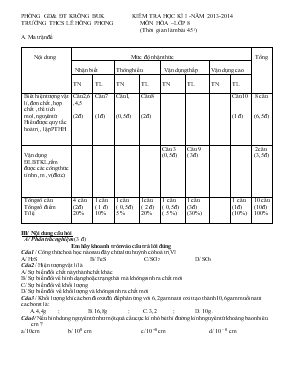
PHÒNG GD& ĐT KRÔNG BUK KIỂM TRA HỌC KÌ I -NĂM 2013-2014 TRƯỜNG THCS LÊ HỒNG PHONG MÔN HÓA –LỚP 8 (Thời gian làm bài 45/) A. Ma trận đề Nội dung Mức độ nhận thức Tổng Nhận biết Thông hiểu Vận dụng thấp Vận dụng cao TN TL TN TL TN TL TN TL Biết hiện tượng vật lí ,đơn chất ,hợp chất ,thể tích mol,nguyên tử Hiểu được quy tắc hoá trị , lập PTHH Câu2,6,4,5 (2đ) Câu7 (1đ) Câu1, (0,5đ ) Câu8 (2đ) Câu10 (1 đ) 8 câu (6,5đ) Vận dụng ĐLBTKL,nắm được các công thức tính n ,m ,v (đktc) Câu 3 (0,5đ) Câu 9 ( 3đ) 2câu (3,5đ ) Tổng số câu Tổng số điểm Tỉ lệ 4 câu (2đ) 20% 1 câu ( 1 đ) 10% 1 câu ( 0,5đ) 5 % 1câu ( 2 đ) 20% 1 câu ( 0,5đ) ( 5 %) 1 câu (3đ) (30%) 1 câu (1đ) (10%) 10 câu (10đ ) 100% III/ Nội dung câu hỏi A/ Phần trắc nghiệm (3 đ) Em hãy khoanh tròn vào câu trả lời đúng Câu1 / Công thức hoá học nào sau đây chứa lưu huỳnh có hoá trị VI A/ H2S B/ FeS C/ SO2 D/ SO3 Câu2 / Hiện tượng vật lí là A/ Sự biến đổi chất này thành chất khác B/ Sự biến đổi về hình dạng hoặc trạng thái mà không sinh ra chất mới C/ Sự biến đổi về khối lượng D/ Sự biến đổi về khối lượng và không sinh ra chất mới Câu3 / Khối lượng khí cácbon đioxit đủ để phản ứng với 6,2 gam natri oxit tạo thành 10,6 gam muối natri cacbonat là: A.4,4g ; B.16,8g ; C. 3,2 ; D. 10g . Câu4/ Nếu hình dung nguyên tử như một quả cầu cực kì nhỏ bé thì đường kính nguyên tử khoảng bao nhiêu cm ? a/10 cm b/ 10 8 cm c/ 10 +8 cm d/ 10 – 8 cm Câu5/ Viết 5Ca ,ý nghĩa của cách viết này là: a/ 5 nguyên tố Canxi b/ 5 nguyên tử caxi c/ 5 đơn chất canxi d/ Cả b,c đều đúng Câu6/ Phát biểu nào sau đây là đúng : A. Thể tích mol chất khí là thể tích chiếm bởi 1 mol nguyên tử chất khí. B. Thể tích mol chất khí là thể tích chiếm bởi N phân tử chất khí. C. thể tích mol chất khí là thể tích chiếm bởi N nguyêntử chất khí D.Thể tích mol chất khí là thể tích chiếm bởi 1 gam chất khí. B. Phần tự luận : Câu7 / Đơn chất , hợp chất là gì , cho ví dụ (1 đ) Câu 8/ (2đ ) Cho sơ đồ các phản ứng sau : A.Fe + Br2 --- → Fe Br3 B. Al + CuO --- → Al2O3 + Cu C. BaCl2 + AgNO3 ---→ AgCl + Ba (NO3)2 D. C4H10 + O2 ---→ CO2 + H2O Lập phương trình hoá học ,cho biết tỷ lệ số nguyên tử , số phân tử giữa các chất trong phản ứng Câu9 / (3 đ) Khi cho khí hi đro (H2) đi qua bột sắt (III) o xit có công thức Fe2O3 nung nóng thì thu được sắt (Fe) và nước (H2O) a. Viết phương trình phản ứng xảy ra. b. Nếu sau phản ứng ta thu được 22,4gam sắt thì khối lượng sắt (III) o xít tham gia là bao nhiêu gam c. Tính thể tích khí hiđrô cần cho phản ứng ở ĐKTC Câu10 / Một hợp chất X có tỷ lệ về khối lượng các nguyên tố là mMg : m C : m O = 2 : 1: 4 , biết M X = 84 đvC . Xác định công thức phân tử của hợp chất ( X) . (1 đ) HƯỚNG DẪN CHẤM A/ Phần trắc nghiệm (3 đ) Mỗi câu đúng đạt 0,5 điểm Câu 1 2 3 4 5 6 Đáp án D B A D B B B/ Phần tự luận (7 đ) Câu7 / * Đơn chất là những chất được tạo nên từ một nguyên tố hoá học ( 0,25 đ ) - Ví dụ : H 2 , C ( 0,25 đ) * Hợp chất là những chất được tạo nên từ hai nguyên tố hoá học trở lên (0,25 đ) - Ví dụ : nước , khí cabonic (0,25 đ) Câu8 / a. 2 Fe + 3 Br2 2 Fe Br3 (0,25 ) * Tỷ lệ : 2 : 3 : 2 (0,25 đ) b. 2 Al + 3CuO → Al2O3 + 3Cu (0,25 đ) * Tỷ lệ : 2 : 3: 1: 3 (0,25 ) c. BaCl2 + 2AgNO3 → 2AgCl + Ba (NO3)2 (0,25 đ) * tỷ lệ : 1 : 2 : 2 : 1 (0,25 đ) d. 2C4H10 + 13 O2 to 8 CO2 + 10 H2O (0,25 đ) * Tỷ lệ 2: 13 : 8 : 10 (0,25 ) Câu9/ a/ PT : Fe2O3 + 3H2 to 2Fe + 3H2O (0,5 ) b/ Ta có n Fe = 2,24 / 56 = 0,4 (mol ) (0,5 đ) Theo PT cứ 1mol Fe2O3 sinh ra 2 mol Fe (0,25) Theo ĐB cứ x mol Fe2O 3 sinh ra 0,4 mol Fe → n Fe2O 3 = 0,4 .1 / 2 = 0,2 (mol ) (0,25 đ) m Fe2O 3 = 0,2 . 160 = 32 (g) (0,25 ) c/ Theo PT cứ 3mol H2 sinh ra 2 mol Fe (0,25 đ) Theo ĐB cứ x mol H 2 sinh ra 0,4 mol Fe n H2 = 0,4 .3 /2 = 0,6 (mol) (0,5 ) V H2 = 0,6 .22,4 = 13,44 ( l ) (0,5 ) Câu 10/ Lập tỷ lệ : x: y : z = 2/24 : 1/12 : 4/16 = 1/3 : 1/3 : 1 = 1:1:3 (0,25 ) → Công thức nguyên của X Là : ( MgCO 3 ) n Mà Mx = (24 + 12 +48 ) n = 84 (0,25 ) → n = 1 ( 0,25 đ) Vậy công thức phân tử là :MgCO3 ( 0,25 ) Duyệt của tổ chuyên môn GV ra đề Tổ trưởng Bùi Thị Hồng Hạnh Nguyễn Thị Hoàng Thư
Tài liệu đính kèm:
 Matran_de_va_dap_an_thi_HKI.doc
Matran_de_va_dap_an_thi_HKI.doc





