Đề kiểm tra môn Hóa học Lớp 8 - Năm học 2016-2017 - Trường THCS Tân Đức (Có đáp án)
Bạn đang xem tài liệu "Đề kiểm tra môn Hóa học Lớp 8 - Năm học 2016-2017 - Trường THCS Tân Đức (Có đáp án)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
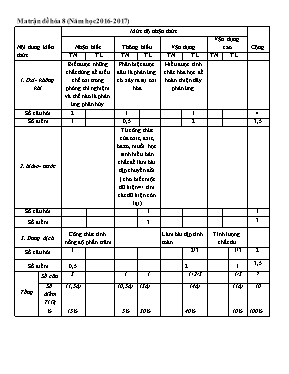
Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng Vận dụng cao TN TL TN TL TN TL TN TL 1. Oxi- không khí Biết được những chất dùng để điều chế oxi trong phòng thí nghiệm và thế nào là phản ứng phân hủy Phân biệt được đâu là phản ứng có xảy ra sự oxi hóa Hiểu được tính chât hóa học để hoàn thiện dãy phản ứng Số câu hỏi 2 1 1 4 Số điểm 1 0,5 2 3,5 2. hidro- nước Từ công thức của oxit, axit, bazo, muối học sinh hiểu bản chất để làm bài tập chuyển đổi ( cho biết một dữ kiện=> tìm các dữ kiện còn lại) Số câu hỏi 1 1 Số điểm 3 3 3. Dung dịch Công thức tính nồng độ phần trăm Làm bài tập tính toán Tính lượng chất dư Số câu hỏi 1 2/3 1/3 2 Số điểm 0,5 2 1 3,5 Tổng Số câu 3 1 1 1+2/3 1/3 7 Số điểm Tỉ lệ % (1,5đ) 15% (0,5đ) 5% (3đ) 30% (4đ) 40% (1đ) 10% 10 100% Ma trận đề hóa 8 (Năm học 2016- 2017) PHÒNG GD&ĐT PHÚ BÌNH ĐỀ KIỂM TRA HỌC KÌ II TRƯỜNG THCS TÂN ĐỨC NĂM HỌC 2016- 2017 MÔN: HÓA HỌC 8 Họ và tên:.................. ........ (Thời gian làm bài: 45 phút, không kể thời gian giao đề) Lớp:........ Điểm: ĐỀ BÀI PHẦN I: Trắc nghiệm (2 điểm). Hãy khoanh tròn một trong các chữ A, B, C, D trước phương án chọn đúng. Câu 1: Hòa tan 10 gam muối ăn vào 40 gam nước. Nồng độ phần trăm của dung dịch thu được là: A. 25% B. 20% C. 2,5% D. 2% Câu 2: Ph¶n øng ho¸ häc cã x¶y ra sù oxi ho¸ lµ: A. MgCO3 MgO + CO2 B. CaO + H2O Ca(OH)2 C. 3Fe + 2O2 Fe3O4 D. K2SO4 + BaCl2 BaSO4 + 2KCl Câu 3: Những chất được dùng để điều chế oxi trong phòng thí nghiệm là: A. KMnO4 và không khí. B. KMnO4 và H2O. C. KClO3 và CaCO3 . D. KMnO4 và KClO3. Câu 4: . Phản ứng nào dưới đây là phản ứng phân hủy. A. Cu(OH)2 CuO + H2O . B. CO2 + Ca(OH)2 CaCO3 + H2O. C. 3Fe + 2O2 Fe3O4 D. CuO + H2 Cu + H2O PHẦN II: Tự Luận (8 điểm) Câu 5.(3đ) Điền công thức hóa học của chất hoặc tên gọi cho phù hợp vào ô trống: CTHH của oxit CTHH của axit CTHH của Bazo CTHH của muối Tên gọi của muối Kaliphotphat SO3 Fe(OH)2 MgO HCl Canxi cacbonat Câu 6. (2đ) Viết phương trình biểu diễn chuyển hóa sau: C CO2 CaCO3 CaO Ca(OH)2 Câu 7. (3đ) Cho 6,5 gam kẽm tác dụng với 100 gam dd HCl 14,6% a, Viết phương trình phản ứng xảy ra b, Chất nào còn dư sau phản ứng và dư bao nhiêu ? c, Tính thể tích khí hiđro thoát ra (ở ĐKTC) BÀI LÀM. .................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................. .................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................. .................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................. .................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................. .................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................. HƯỚNG DẪN CHẤM ĐỀ KIỂM TRA HỌC KÌ II NĂM HỌC 2016- 2017 MÔN: HÓA HỌC 8 Đáp án Biểu điểm Trắc nghiệm D A B Học sinh khoanh vào câu đúng C 1. A 2. 3. 4. Mỗi câu đúng được 0,5 điểm Tự luận Câu 5 CTHH của oxit CTHH của axit CTHH của bazo CTHH của muối Tên gọi của muối P2O5 hoặc K2O H3PO4 KOH K3PO4 Kaliphotphat SO3 H2SO4 Fe(OH)2 FeSO4 Sắt(II) sunfat MgO HCl Mg(OH)2 MgCl2 Magie clorua CaO hoặc CO2 H2CO3 Ca(OH)2 CaCO3 Can xi cacbonat 3 điểm Mỗi ý đúng được 0,2 điểm Câu 6 C+ O2 CO2 CaO + CO2 CaCO3 CaCO3 CaO + CO2\ CaO + H2O Ca(OH)2 2 điểm Mỗi ý đúng được 0,5 điểm Câu 7 PTHH Zn + 2HCl ZnCl2 + H2 b. HS tính được: nZn= 0,1 mol nHCl = 0,4 mol so sánh số mol của Zn và HCl-> HCl dư nHCl dư = 0,2 mol => mHCl dư = 0,2. 36,5 = 7,3 (g) c. Tính được: nH= 0,1 mol => VH= n.22,4= 0,1. 22,4= 2,24 (l) 3 điểm 0,5 đ 1,5 đ 1 đ (Học sinh giải theo cách khác- nếu đúng- vẫn cho điểm tối đa)
Tài liệu đính kèm:
 de_kiem_tra_mon_hoa_hoc_lop_8_nam_hoc_2016_2017_truong_thcs.docx
de_kiem_tra_mon_hoa_hoc_lop_8_nam_hoc_2016_2017_truong_thcs.docx






