Đề 2 kiểm tra 1 tiết (bài số 2) lớp 10 năm học 2014 - 2015 môn: Hóa học
Bạn đang xem tài liệu "Đề 2 kiểm tra 1 tiết (bài số 2) lớp 10 năm học 2014 - 2015 môn: Hóa học", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
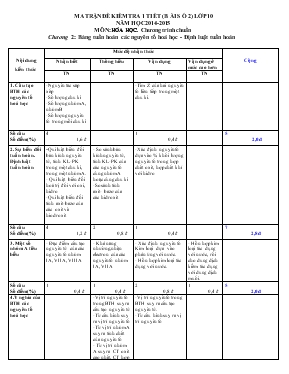
MA TRẬN ĐỀ KIỂM TRA 1 TI ẾT (B ÀI S Ố 2) LỚP 10 NĂM HỌC 2014-2015 MÔN: HOÙA HOÏC. Chương trình chuẩn Chương 2: Bảng tuần hoàn các nguyên tố hoá học - Định luật tuần hoàn Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng Vận dụng ở mức cao hơn TN TN TN TN 1. Cấu tạo BTH các nguyên tố hoá học -Nguyên tắc sắp xếp -Số lượng chu kì -Số lượng nhóm A, nhóm B -Số lượng nguyên tố trong mỗi chu kì -Tìm Z của hai nguyên tố liên tiếp trong một chu kì. Số câu Số điểm(%) 4 1,6 đ 1 0,4đ 5 2,0đ 2. Sự biến đổi tuần hoàn. Định luật tuần hoàn -Qui luật biến đổi bán kính nguyên tử, tính KL-PK trong một chu kì, trong một nhóm A. - Qui luật biến đổi hoá trị đối với oxi, hidro -Qui luật biến đổi tính axit-bazơ của các oxit và hiodroxit - So sánh bán kính nguyên tử, tính KL-PK của các nguyên tố cùng nhóm A hoặc cùng chu kì -So sánh tính axit- bazơ của các hidroxit -Xác định nguyên tố dựa vào % khối lượng nguyên tố trong hợp chất oxit, hợp chất khí với hidro Số câu Số điểm(%) 4 1,2 đ 2 0,8 đ 1 0,4đ 7 2,8đ 3. Một số nhóm A tiêu biểu - Đặc điểm cấu tạo nguyên tử của các nguyên tố nhóm IA, VIIA, VIIIA - Khả năng nhường, nhận electron của các nguyên tố nhóm IA, VIIA - Xác định nguyên tố Kim loại dựa vào phản ứng với nước. - Hỗn hợp kim loại tác dụng với nước. - Hỗn hợp kim loại tác dụng với nước, rồi cho dung dịch kiềm tác dụng với dung dịch muối. Số câu Số điểm(%) 1 0,4 đ 1 0,4 đ 2 0,8 đ 1 0,4 đ 5 2,0đ 4.Ý nghĩa của BTH các nguyên tố hoá học -Vị trí nguyên tố trong BTH suy ra cấu tạo nguyên tử -Từ cấu hình suy ra vị trí nguyên tố -Từ vị trí nhóm A suy ra tính chất của nguyên tố - Từ vị trí nhóm A suy ra CT oxit cao nhất, CT hợp chất với hidro. -Vị trí nguyên tố trong BTH suy ra cấu tạo nguyên tử. -Từ cấu hình suy ra vị trí nguyên tố Số câu Số điểm(%) 5 2,0 đ 3 1,2 đ 8 3,2đ Tổng số câu Tổng số điểm 9 3,6 đ 8 3,2đ 7 2,8đ 1 0,4 đ 25 10đ Họ, tên học sinh: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . Lớp: . . . . . . . . . . . SỞ GD-ĐT NINH THUẬN Trường THPT Trường Chinh ********* (đề kiểm tra có 2 trang) ĐỀ KIỂM TRA 1 TI ẾT (B ÀI S Ố 2) LỚP 10 NĂM HỌC 2014-2015 MÔN: HOÙA HOÏC. Chương trình chuẩn Thời gian làm bài: 45 phút (không kể thời gian phát đề) Mã đề 132 ĐỀ: Cho nguyên tử khối của các nguyên tố : H = 1; O = 16; Cl=35,5; Li=7; Na = 23; K=39; Fe=56; Rb=86; Ba=137 Câu 1: Nguyên tố M ở chu kỳ 2, nhóm VA. Số hạt proton có trong nguyên tử M là: A. 7 B. 8 C. 5 D. 6 Câu 2: Trong bảng tuần hoàn, số chu kỳ nhỏ và chu kỳ lớn lần lượt là: A. 2 và 5 B. 4 và 3 C. 3 và 4 D. 3 và 2 Câu 3: Trong một chu kỳ, theo chiều tăng của điện tích hạt nhân, thì hóa trị cao nhất của các nguyên tố trong hợp chất với oxi sẽ? A. tăng từ 1 đến 7 B. Giảm từ 7 đến 1 C. Giảm từ 4 đến 1 D. Tăng từ 1 đến 4 Câu 4: Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kỳ (ZA<ZB). Tổng số hạt proton trong 2 nguyên tử A và B là 31. Tìm số hiệu nguyên tử của nguyên tố A? A. 10 B. 15 C. 16 D. 14 Câu 5: Nguyên tố X ở chu kỳ 3, nhóm IIIA. Cấu hình electron của nguyên tử X là : A. 1s2 2s2 2p6 3s2 3p1 B. 1s2 2s2 2p6 3s2 3p3 C. 1s2 2s2 2p1 D. 1s2 2s2 2p6 3s2 3p6 Câu 6: Nguyên tố R có Z=17. Hóa trị của nguyên tố R trong hợp chất khí với hidro là: A. 2 B. 1 C. 3 D. 4 Câu 7: Số hiệu nguyên tử của các nguyên tố X(Z=7) ; Y(Z=12) ; M (Z=18) ; Q(Z=15). Nhận xét nào đúng? A. có 2 nguyên tố ở cùng một chu kỳ B. có 2 nguyên tố ở cùng một nhóm A C. có 2 nguyên tố là kim loại D. có 2 nguyên tố là khí hiếm Câu 8: Để đạt được cấu hình electron bền vững của khí hiếm, thì trong phản ứng hóa học, nguyên tử của các nguyên tố kim loại kiềm sẽ nhường (hay nhận) bao nhiêu electron? A. nhường 2e B. nhận 1e C. nhường 1e D. nhận 2e Câu 9: Trong các hidroxit sau, hidroxit có tính axit mạnh nhất là: A. H2SiO3 B. H2SO4 C. HClO4 D. H3PO4 Câu 10: Trong bảng tuần hoàn, các nguyên tố ở cùng một chu kỳ sẽ có cùng: A. Số electron trong nguyên tử B. Số phân lớp electron C. Số electron ở lớp ngoài cùng D. Số lớp electron Câu 11: Nguyên tố R có cấu hình electron ở lớp ngoài cùng là ns2np2. Công thức hợp chất khí của R với hidro là : A. RH2 B. RH C. RH4 D. RH3 Câu 12: Cấu hình electron lớp ngoài cùng của các nguyên tố nhóm halogen là: A. ns2 np1 B. ns2 np3 C. ns2 np5 D. ns2 np6 Câu 13: Nguyên tử có giá trị độ âm điện lớn nhất trong bảng tuần hoàn là: A. H B. F C. O D. Cl Câu 14: Nguyên tố R tạo được hợp chất khí với hidro là RH3. Trong công thức oxit mà R có hóa trị cao nhất, thì R chiếm 65,21% về khối lượng. Tìm nguyên tử khối của nguyên tố R? A. 73 B. 32 C. 14 D. 75 Câu 15: Hòa tan hết 11,45g hỗn hợp X gồm (Na và Ba) vào nước, thu được 3,36 lít khí hidro (đktc). Tính phần trăm khối lượng của Na trong hỗn hợp X? A. 40,17% B. 45,17% C. 30,17% D. 35,17% Câu 16: Trong bảng tuần hoàn, số nguyên tố có trong chu kỳ 3 và 5 lần lượt là: A. 18 và 18 B. 8 và 18 C. 18 và 32 D. 8 và 8 Câu 17: Trong bảng tuần hoàn, nhóm nguyên tố nào sau đây chỉ có các nguyên tố s? A. tất cả các nhóm B B. IVA và VA C. VIIA và VIIIA D. IA và IIA Câu 18: Trong một nhóm A, theo chiều tăng của điện tích hạt nhân, thì? A. bán kính nguyên tử tăng và tính kim loại tăng B. bán kính nguyên tử giảm và tính kim loại tăng C. bán kính nguyên tử tăng và tính kim loại giảm D. bán kính nguyên tử giảm và tính kim loại giảm Câu 19: Theo quy luật biến đổi tính chất của các đơn chất, thì? A. Kim loại mạnh nhất là nhôm B. Kim loại mạnh nhất là liti C. phi kim mạnh nhất là flo D. Phi kim mạnh nhất là oxi Câu 20: Cho các nguyên tố M(Z=16), X(Z=12), Y(Z=8), R(Z=20). Hãy xếp các nguyên tố trên theo chiều bán kính nguyên tử tăng dần? A. X, Y, R, M B. Y, X, M, R C. R, M, X, Y D. Y, M, X, R Câu 21: Nguyên tử của nguyên tố M có 2 lớp electron, có 7 electron ở lớp ngoài cùng. Vị trí của nguyên tố M trong bảng tuần hoàn là: A. ô thứ 7, chu kỳ 2, nhóm VIA B. ô thứ 9, chu kỳ 2, nhóm VIIA C. ô thứ 8, chu kỳ 3, nhóm VIIA D. ô thứ 12, chu kỳ 3, nhóm IIA Câu 22: Nguyên tử của nguyên tố X có tổng số electrron trong các phân lớp p là 10. Vị trí của nguyên tố X trong bảng tuần hoàn là: A. ô thứ 10, chu kỳ 2, nhóm VIIIA B. ô thứ 16, chu kỳ 3, nhóm VIA C. ô thứ 14, chu kỳ 3, nhóm IVA D. ô thứ 18, chu kỳ 3, nhóm VA Câu 23: Nguyên tố R ở nhóm IVA. Công thức oxit cao nhất của R là: A. RO3 B. R2O3 C. R2O5 D. RO2 Câu 24: Hòa tan hết 6,24g một kim loại nhóm IA vào nước, thu được 1,792 lít khí hidro (đktc). Tìm kim loại? A. Na B. Rb C. Li D. K Câu 25: Hòa tan hết hỗn hợp X gồm (K, Na và Ba) vào nước, thu được 13,44 lít khí hidro (đktc) và dung dịch Y. Cho FeCl3 dư vào dung dịch Y, thu được kết tủa Z. Đem nung kết tủa Z, thu được m gam chất rắn T. Các phản ứng đều xảy ra hoàn toàn. Giá trị của m là: A. 32 B. 16 C. 8 D. 96 ----------------------------------------------- ----------- HẾT ---------- SỞ GD-ĐT NINH THUẬN Trường THPT Trường Chinh ********* ĐỀ KIỂM TRA 1 TI ẾT (B ÀI S Ố 2) LỚP 10 NĂM HỌC 2014-2015 MÔN: HOÙA HOÏC. Chương trình chuẩn ĐÁP ÁN, HƯỚNG DẪN CHẤM VÀ BIỂU ĐIỂM (MỖI CÂU ĐÚNG 0,4 ĐIỂM) Câu 132 209 357 485 1 A D B A 2 C D C D 3 A C A C 4 B C C C 5 A C B C 6 B B B A 7 B D A D 8 C C A A 9 C A D A 10 D D C A 11 C A C C 12 C B A A 13 B A A D 14 D D B B 15 A B D B 16 B A A B 17 D A A B 18 A C B A 19 C D C D 20 D B D C 21 B C D C 22 B B D B 23 D D B D 24 D B C B 25 A B C A
Tài liệu đính kèm:
 Hoa_Ch_(TRUONGCHINH)2-10.doc
Hoa_Ch_(TRUONGCHINH)2-10.doc





