Ma trận đề kiểm tra học kỳ I Hóa học 9 năm học: 2016 – 2017
Bạn đang xem tài liệu "Ma trận đề kiểm tra học kỳ I Hóa học 9 năm học: 2016 – 2017", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
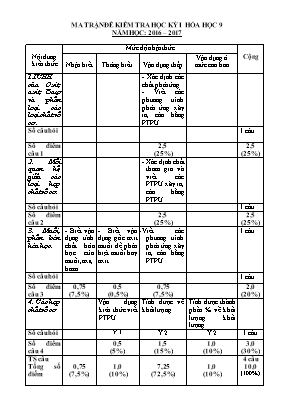
MA TRẬN ĐỀ KIỂM TRA HỌC KỲ I HÓA HỌC 9 NĂM HỌC: 2016 – 2017 Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng thấp Vận dụng ở mức cao hơn 1.TCHH của Oxit, axit, Bazơ và phân loại các loại chất vô cơ . - Xác định các chất phản ứng - Viết các phương trình phản ứng xãy ra, cân bằng PTPU Số câu hỏi 1 câu Số điểm câu 1 2,5 (25%) 2,5 (25%) 2. Mối quan hệ giữa các loại hợp chất vô cơ. Xác định chất tham gia và viết các PTPU xãy ra, cân bằng PTPU Số câu hỏi 1 câu Số điểm câu 2 2,5 (25%) 2,5 (25%) 3. Muối, phân bón hóa học. - Biết vận dụng tính chất hóa học của muối,axit, bazo. - Biết vận dụng gốc axit muối để phân biệt muối hay axit. Viết các phương trình phản ứng xãy ra, cân bằng PTPU 1 câu Số câu hỏi 1 câu Số điểm câu 3 0,75 (7,5%) 0,5 (0,5%) 0,75 (7,5%) 2,0 (20%) 4. Các hợp chất vô cơ Vận dụng kiên thức viết PTPU Tính được về khối lượng. Tính được thành phần % về khối lượng. khối lượng Số câu hỏi Ý 1 Ý 2 Ý 2 1 câu Số điểm câu 4 0,5 (5%) 1,5 (15%) 1,0 (10%) 3,0 (30%) TS câu Tổng số điểm 0,75 (7,5%) 1,0 (10%) 7,25 (72,5%) 1,0 (10%) 4 câu 10,0 (100%) 0,5 (5%) 4 10,0 (100%) TRƯỜNG THCS ĐỀ KIỂM TRA HỌC KỲ I MÔN: HÓA HỌC 9. NĂM HỌC 2016 - 2017 Thời gian 45 phút (Không kể thời gian giao đề) ĐỀ B Câu 1:( 2,5 điểm). Cho các chất sau: K2O, FeCl2 , H2SO4, Ca(OH)2 . a, Chất nào tác dụng đ ược với NaOH. b, Chất nào tác dụng đ ược với H2SO4. Viết các ph ư ơng trình phản ứng xãy ra (nếu có) ? Câu 2:(2,5 điểm). Viết các phương trình phản ứng thực hiện dãy biến hóa theo sơ đồ sau: Al (1) AlCl3 (2) Al(OH)3 (3) Al2O3 (4) Al2(SO4)3 (5) AlCl3 Câu 3:( 2,0 điểm). Có 4 lọ đựng 4 dung dịch KOH, H2SO4,HCl và NaCl bị mất nhãn. Hãy bằng phương pháp hóa học nhận biết các chất đựng trong mổi lọ? Câu 4:( 3,0 điểm). Cho 40 gam hổn hợp 2 kim loại Cu và Zn tác dụng với dung dịch axit sunfuric loãng, sau phản ứng thu được dung dịch muối sunfat và 11,2 lít khí hiđro (ở đktc). Viết phương trình hóa học xảy ra. Tính thành phần phần trăm theo khối lượng của mổi kim loại có trong hổn hợp trên? ( Cu = 64, Zn = 65, H= 1, O = 16, S= 32 ). TRƯỜNG THCS ĐỀ KIỂM TRA HỌC KỲ I MÔN: HÓA HỌC 9. NĂM HỌC 2016 - 2017 Thời gian 45 phút (Không kể thời gian giao đề) ĐỀ A Câu 1:( 2,5 điểm). Cho các chất sau: Na2O, ZnCl2 , HCl, Ca(OH)2 . a, Chất nào tác dụng đ ược với NaOH. b, Chất nào tác dụng đ ược với H2SO4. Viết các ph ư ơng trình phản ứng xãy ra (nếu có) ? Câu 2:(2,5 điểm.) Viết các phương trình phản ứng thực hiện dãy biến hóa theo sơ đồ sau: Fe (1) FeCl3 (2) Fe(OH)3 (3) Fe2O3 (4) Fe2(SO4)3 (5) FeCl3 Câu 3:( 2,0 điểm). Có 4 lọ đựng 4 dung dịch NaOH, H2SO4,NaCl và Na2SO4 bị mất nhãn. Hãy bằng phương pháp hóa học nhận biết các chất đựng trong mổi lọ? Câu 4:( 3,0 điểm.) Cho 40 gam hổn hợp 2 kim loại Cu và Fe tác dụng với dung dịch axit sunfuric loãng, sau phản ứng thu được dung dịch muối sunfat và 6,72 lít khí hiđro (ở đktc). Viết phương trình hóa học xảy ra. . Tính thành phần phần trăm theo khối lượng của mổi kim loại có trong hổn hợp trên? ( Cu = 64, Fe = 56, H= 1, O = 16, S= 32 ). ĐÁP ÁN HÓA 9 HỌC KỲ I Năm học: 2016 – 2017 Đề A TT Đáp án Biểu điểm Câu 1 2,5 điểm 1. ZnCl2 + 2 NaOH Zn(OH)2 + 2 NaCl 2. HCl + NaOH NaCl + H2O 3. Na2O + H2SO4 Na2SO4+ H2O 4. ZnCl2 + H2SO4 ZnSO4+ 2HCl 5. Ca(OH)2 + H2SO4 CaSO4 + 2H2O 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm Câu 2 2,5 điểm 1. 2Fe + 3Cl2 2FeCl3 2. FeCl3 + 3NaOH Fe(OH)3 + 3NaCl 3. 2 Fe(OH)3 Fe2O3 + 3 H2O 4. Fe2O3 + 2 H2SO4 Fe2(SO4)3 + H2O 5. Fe2(SO4)3 + 3 BaCl2 2 FeCl3 + 3BaSO4 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm Câu 3 2,0 điểm - Dùng quỳ tím nếu: Ngã màu xanh: NaOH Ngã màu đỏ: H2SO4 Không ngã màu: NaCl, Na2SO4 - Dùng BaCl2 cho vào 2 dung dịch muối, nếu xuất hiện màu trắng đó là : Na2SO4 Na2SO4 + BaCl2 BaSO4 + 2 NaCl Chất còn lại NaCl. 0,25 điểm 0,25 điểm 0,25 điểm 0,5 điểm 0,5 điểm 0,25 điểm Câu 4 3,0 điểm nH2 = 6,72/22,4 = 0,3 (mol) PT: Fe + H2SO4 FeSO4 + H2 Theo PT: nH2 = nFe = 0,3 mol. mFe = 0.3 x 56 = 16,8 gam. mCu = 40 – 16,8 = 23,2 gam. %Fe = (16,8 x100%)/40 = 42 % => %Cu = 58 % 0, 5 điểm 0, 5 điểm 0,5 điểm 0, 5 điểm 0,25 điểm 0,5 điểm 0,25 điểm Ghi chú: - Viết PTPU thiếu điều kiện cho ½ số điểm theo quy định. - Thí sinh có thể giải cách khác đúng vẩn cho điểm tối đa. ĐÁP ÁN HÓA 9 HỌC KỲ I Năm học: 2016 – 2017 Đề B TT Đáp án Biểu điểm Câu 1 2,5 điểm 1. FeCl2 + 2 NaOH Fe(OH)2 + 2 NaCl 2. H2SO4 + 2 NaOH Na2SO4 + H2O 3. K2O + H2SO4 K2SO4+ H2O 4. FeCl2 + H2SO4 FeSO4+ 2HCl 5. Ca(OH)2 + H2SO4 CaSO4 + 2H2O 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm Câu 2 2,5 điểm 1. 2Al + 3Cl2 2 AlCl3 2. AlCl3 + 3NaOH Al (OH)3 + 3NaCl 3. 2 Al(OH)3 Al2O3 + 3 H2O 4. Al2O3 + 2 H2SO4 Al2(SO4)3 + H2O 5. Al2(SO4)3 + 3 BaCl2 2 AlCl3 + 3BaSO4 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm Câu 3 2,0 điểm - Dùng quỳ tím nếu: Ngã màu xanh: KOH Ngã màu đỏ: H2SO4 , HCl Không ngã màu: NaCl. - Dùng BaCl2 cho vào 2 dung dịch muối, nếu xuất hiện màu trắng đó là : H2SO4 H2SO4 + BaCl2 BaSO4 + 2 HCl Chất còn lại HCl. 0,25 điểm 0,25 điểm 0,25 điểm 0,5 điểm 0,5 điểm 0,25 điểm Câu 4 3,0 điểm nH2 = 11,2/22,4 = 0,5 (mol) PT: Fe + H2SO4 FeSO4 + H2 Theo PT: nH2 = nFe = 0,5 mol. mFe = 0.5 x 56 = 28 gam. mCu = 40 – 28 = 12 gam. %Fe = (28 x100%)/40 = 70 % => %Cu = 30 % 0, 5 điểm 0, 5 điểm 0,5 điểm 0, 5 điểm 0,25 điểm 0,5 điểm 0,25 điểm Ghi chú: - Viết PTPU thiếu điều kiện cho ½ số điểm theo quy định. - Thí sinh có thể giải cách khác đúng vẩn cho điểm tối đa.
Tài liệu đính kèm:
 DE_DA_HOA9_HK1_CO_MA_TRAN.doc
DE_DA_HOA9_HK1_CO_MA_TRAN.doc





