Ma trận đề kiểm tra học kì I môn Hoá 9 – Năm học: 2016 - 2017 - Trường THCS Huỳnh Thúc Kháng
Bạn đang xem tài liệu "Ma trận đề kiểm tra học kì I môn Hoá 9 – Năm học: 2016 - 2017 - Trường THCS Huỳnh Thúc Kháng", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
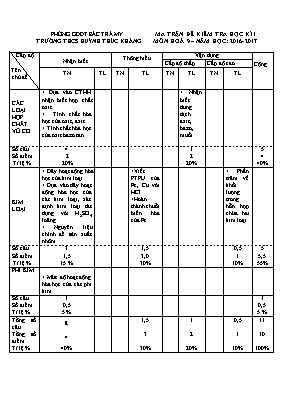
PHÒNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG MA TRẬN ĐỀ KIỂM TRA HỌC KÌ I MÔN HOÁ 9 – NĂM HỌC: 2016- 2017 Cấp độ Tên chủ đề Nhận biết Thông hiểu Vận dụng Cộng Cấp độ thấp Cấp độ cao TN TL TN TL TN TL TN TL CÁC LOẠI HỢP CHẤT VÔ CƠ + Dựa vào CTHH nhận biết hợp chất oxit. + Tính chất hóa học của oxit, axit. + Tính chất hóa học của oxit bazo tan. + Nhận biết dung dịch axit, bazo, muối. Số câu 4 1 5 Số điểm Tỉ lệ % 2 20% 2 20% 4 40% KIM LOẠI + Dãy hoạt động hóa học của kim loại. + Dựa vào dãy hoạt động hóa học của các kim loại, xác định kim loại tác dụng với H2SO4 loãng. + Nguyên liệu chính để sản xuất nhôm +Viết PTPU của Fe, Cu với HCl +Hoàn thành chuỗi biến hóa của Fe. + Phần trăm về khối lượng trong hỗn hợp chứa hai kim loại Số câu Số điểm Tỉ lệ % 3 1,5 15 % 1,5 3,0 30% 0,5 1 10% 5 5,5 55% PHI KIM + Mức độ hoạt động hóa học của các phi kim. Số câu Số điểm Tỉ lệ % 1 0,5 5 % 1 0,5 5 % Tổng số câu 8 1,5 1 0,5 11 Tổng số điểm 4 3 2 1 10 Tỉ lệ % 40% 30% 20% 10% 100% PHÒNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG Họ và tên:..................................................... Lớp:..................... ĐỀ KIỂM TRA HỌC KỲ I Năm học : 2016 - 2017 Môn : Hóa Học 9 Thời gian : 45 phút (không kể thời gian phát đề) Điểm: Lời phê của giáo viên: I. Trắc nghiệm: (4 điểm) Khoanh tròn vào đáp án đúng: Câu 1: Chất tác dụng với nước tạo ra dung dịch bazơ là: A. CO2 B. Na2O C. SO2 D. K2O Câu 2: Dãy các nguyên tố được sắp xếp đúng theo chiều tính phi kim tăng dần: A . O, F, P B. P , O, F C. F, O, P D. O, P, F Câu 3: Dãy chất sau đây chỉ gồm các oxit: A. MgO, Ba(OH)2, CaSO4, HCl B. MgO, CaO, CuO, FeO C. SO2, CO2, NaOH, CaSO4 D. CaO, Ba(OH)2, MgSO4, BaO Câu 4: Dãy kim loại được sắp xếp theo chiều hoạt động hóa học tăng dần: A. K, Al, Mg, Cu, Fe B. Cu, Fe, Mg, Al, K C. Cu, Fe, Al, Mg, K D. K, Cu, Al, Mg, Fe Câu 5: Oxit khi tác dụng với nước tạo ra dung dịch axit sunfuric là: A. CO2 B. SO3 C. SO2 D. K2O Câu 6: Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là: A. Mg B. CaCO3 C. Zn D. Na2SO3 Câu 7: Axit H2SO4 loãng không tác dụng với kim loại nào sau đây: A. Cu B. Fe C. Mg D. Ag Câu 8: Nguyên liệu chính để sản xuất nhôm là: A. criolit B. quặng boxit C.điện D. Than chì II/ TỰ LUẬN: (6 điểm ) Câu 1: (2,5 điểm ) Hoàn thành chuỗi biến hóa sau: Fe (1) FeCl3 (2) Fe(OH)3 (3) Fe2O3 (4) Fe2(SO4)3 (5) Fe(OH)3 Câu 2: (2 điểm ) Bằng phương pháp hoá học, hãy nhận biết các dung dịch sau đựng trong các lọ mất nhãn: NaOH, H2SO4, BaCl2, NaCl Câu 3 : (1,5 điểm ) Cho 40g hỗn hợp 2 kim loại Fe và Cu vào dung dịch HCl dư, thu được 11,2 lít khí (đktc). Viết phương trình phản ứng xảy ra? Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu? ( Biết: Cu = 64; Fe = 56; Cl = 35,5; H = 1) -----HẾT----- Phê duyệt của tổ trưởng Người ra đề GVBM Huỳnh Thị Thu Hiền PHÒNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG KIỂM TRA HỌC KÌ I Năm học : 2016 – 2017 Môn : Hóa Học 9 ĐÁP ÁN VÀ BIỂU ĐIỂM: I. Trắc nghiệm: (4 điểm) mỗi câu trả lời đúng được 0,5 điểm Câu 1 2 3 4 5 6 7 8 Đáp án B, D B B C B A, C A, D B II. Tự luận: ( 6 điểm) Câu Đáp án Thang điểm Ghi chú 1 (2,5 đ) (1) 2 Fe + 3 Cl2 t0 2 FeCl3 (2) FeCl3 +3KOH → Fe(OH)3 ↓+ 3 KCl (3) 2 Fe(OH)3 t0 Fe2O3 + 3 H2O (4) Fe2O3 + 3 H2SO4 → Fe2(SO4)3 + 3 H2O (5) Fe2(SO4)3 + 6 NaOH → 2 Fe(OH)3 ↓+ 3 Na2SO4 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm - HS có cách giải khác đúng vẫn cho điểm tối đa 2 (2 đ) - Đánh số thứ tự từ 1 đến 3 trên mỗi lọ mất nhãn - Trích mỗi chất một ít ra làm mẫu thử - Dùng quì tím nhúng vào các mẫu thử: + Mẫu thử nào làm quì tím chuyển sang màu xanh là NaOH + Mẫu thử nào làm quì tím chuyển sang màu đỏ là H2SO4 + Hai mẫu không có hiện tượng gì là: BaCl2, NaCl + Cho một ít dung dịch axit H2SO4 vào 2 mẫu thử còn lại, mẫu nào có hiện tượng kết tủa trắng là BaCl2, mẫu không có hiện tượng gì là NaCl + Phương trình phản ứng: BaCl2 + H2SO4 → BaSO4 ↓ + 2 HCl 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,5 điểm 0,5 điểm 3 (1,5 đ) a/ PTPƯ: Fe + 2HCl à FeCl2 + H2↑ b/ Số mol của H2 thu được là: = V / 22,4 = 11,2/ 22,4= 0,5mol Fe + 2HCl à FeCl2 + H2 1 : 2 : 1 : 1 0,5mol 0,5mol Khối lượng của Fe là: mFe = n. M = 0,5. 56 = 28g Khối lượng của Cu là : mCu = 40 – 28 = 12g Phần trăm về khối lượng của mỗi kim loại là: %mFe = = 70% % mCu = = 30% 0,5 điểm 0,125 điểm 0,125 điểm 0,125 điểm 0,125 điểm 0,25 điểm 0,25 điểm
Tài liệu đính kèm:
 de_KT_hoc_ki_1.doc
de_KT_hoc_ki_1.doc





