Giáo án Tuần 26 - Tiết 52- Kiểm tra 45 phút môn hóa học
Bạn đang xem tài liệu "Giáo án Tuần 26 - Tiết 52- Kiểm tra 45 phút môn hóa học", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
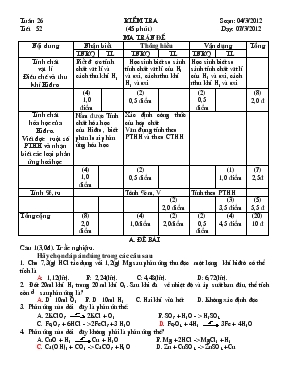
TuÇn 26 KiÓm tra So¹n: 04/3/2012 TiÕt 52 (45 phót) D¹y: 07/3/2012 MA TRẬN ĐÒ Nội dung Nhận biết Thông hiểu Vận dụng Tổng TNKQ TL TNKQ TL TNKQ TL TÝnh chÊt vËt lÝ §iÒu chÕ vµ thu khÝ Hi®ro Biết ®îc tÝnh chÊt vËt lÝ vµ c¸ch thu khÝ H2 Häc sinh biÕt so s¸nh tÝnh chÊt vËt lÝ cña H2 vµ oxi, c¸ch rthu khÝ H2 vµ oxi Häc sinh biÕt so s¸nh tÝnh chÊt vËt lÝ cña H2 vµ oxi, c¸ch rthu khÝ H2 vµ oxi (4) 1,0 điểm (2) 0,5 điểm (2) 0,5 điểm (8) 2,0 đ TÝnh chÊt hãa häc cña Hi®ro. ViÕt ®îc mét sè PTHH vµ nhËn biÕt c¸c lo¹i ph¶n øng ho¸ häc Nắm được TÝnh chÊt hãa häc cña Hi®ro, biÕt ph©n lo¹i ph¶n øng hãa häc X¸c ®Þnh c«ng thøc cña hîp chÊt VËn ®ông tÝnh theo PTHH vµ theo CTHH (4) 1,0 điểm (2) 0,5 điểm (1) 1,0 điểm (7) 2,5đ TÝnh %, m Tính % m, V TÝnh theo PTHH (2) 2,0 điểm (3) 3,5 điểm (5) 5,5 đ Tổng cộng (8) 2,0 điểm (4) 1,0điểm (2) 2,0điểm (2) 0,5 điểm (4) 4,5 điểm (20) 10 đ A. ®Ò bµi C©u 1(3,0®). Trắc nghiệm. Hãy chọn đáp án đúng trong các câu sau: 1. Cho 7,3(g) HCl t¸c dông víi 1,2(g) Mg sau ph¶n øng thu ®îc mét lîng khÝ hi®r« cã thÓ tÝch lµ A: 1,12(lÝt). B: 2,24(lÝt). C: 4,48(lÝt). D: 6,72(lÝt). 2. §èt 20ml khÝ H2 trong 20 ml khÝ O2. Sau khi ®a vÒ nhiÖt ®é vµ ¸p suÊt ban ®Çu, thÓ tÝch cßn d sau ph¶n øng lµ? A. D 10ml O2 B. D 10ml H2 C. Hai khÝ võa hÕt D. Kh«ng x¸c ®Þnh ®îc 3. Ph¶n øng nµo díi ®©y lµ ph¶n øn thÕ: A. 2KClO3 2KCl + O2 B. SO3 +H2O - > H2SO4 C. Fe2O3 + 6HCl - >2FeCl3 +3 H2O D. Fe3O4 + 4H2 3Fe + 4H2O 4. Ph¶n øng nµo díi ®©y kh«ng ph¶i lµ ph¶n øng thÕ? A. CuO + H2 Cu + H2O B. Mg +2HCl -> MgCl2 +H2 C. Ca(OH)2 + CO2 -> CaCO3 +H2O D. Zn + CuSO4 -> ZnSO4 +Cu 5. Trong phßng thÝ nghiÖm cã c¸c kim lo¹i Zn vµ Mg, c¸c dung dÞch axit H2SO4 lo·ng vµ HCl. Muèn ®iÒu chÕ ®îc 1,12lÝt khÝ H2 (®ktc) ph¶i dïng kim lo¹i nµo, axit nµo ®Ó chØ cÇn mét khèi lîng nhá nhÊt? A. Mg vµ H2SO4 B. Mg vµ HCl C. Zn vµ H2SO4 D. Zn vµ HCl 6. Khö 48g ®ång (II) oxit b»ng khÝ hi®ro cho 36,48g ®ång. HiÖu suÊt cña ph¶n øng lµ: A. 90% B. 95% C. 94% D. 85% 7. KhÝ H2 ch¸y trong khÝ O2 t¹o níc theo ph¶n øng: 2H2 + O2 2H2O Muèn thu ®îc 2,25g níc th× thÓ tÝch khÝ H2 (®ktc) cÇn ph¶i ®èt lµ: A. 1,12lÝt B. 2,24lÝt C. 2,8 lÝt D.4,48lÝt 8. D÷ kiÖn cho hai c©u a, b Khö 12g s¾t(III) oxit b»ng khÝ hi®ro a. ThÓ tÝch khÝ hi®ro(®ktc) cÇn dïng lµ: A. 5,04 lÝt B. 1,68 lít C. 10,08 lÝt D. 8,2 lÝt b. Khèi lîng s¾t thu ®îc lµ: A. 18,6g B. 16,8g C.12,6g D. 8,4g 9. ThÓ tÝch khÝ hi®ro tho¸t ra(®ktc) khi cho 16,25g kÏm t¸c dông víi 19,6g Axit sunfuric lµ: A. 22,4 lÝt B. 44,8 lÝt C. 4,48 lÝt D. 2,24 lÝt 10. Cã 11,2 lÝt khÝ H2 (®ktc) tho¸t ra khi cho 56g s¾t t¸c dông víi mét lîng axit clohi®ric. Sè mol axit clohi®ric cÇn thªm tiÕp ®ñ ®Ó hoµ tan hÕt lîng s¾t lµ: A. 0,25mol B. 1,00mol C. 0,75mol D. 0,50mol 11. Dãy kim loại nào sau đây đều tác dụng được với dung dịch HCl tạo khí H2? A. Mg, Zn, Ag, Al. B. Al, Zn, Mg, Hg. C. Cu, Al, Zn, Fe. D. Na, Al, Zn, Mg C©u 2.(3,0®) Hoµn thµnh c¸c ph¬ng tr×nh ph¶n øng sau vµ cho biÕt ®©u lµ ph¶n øng thÕ? 1. P + O2 2. Al + H2SO4 ® + 3. KMnO4 K2MnO4 + MnO2 + 4. FexOy + CO FeO + CO2 5. Al + Fe3O4 Al2O3 + Fe C©u 3(2,0®) DÉn tõ tõ 8,96 lÝt H2 (®ktc) qua m gam oxit s¾t FexOy nung nãng. Sau ph¶n øng ®îc 7,2 gam níc vµ hçn hîp A gåm 2 chÊt r¾n nÆng 28,4 gam (ph¶n øng x¶y ra hoµn toµn). 1/ T×m gi¸ trÞ m? 2/ Hòa tan lượng chất rắn trên vào dung dịch HCl dư thấy thoát ra 6,72 lít khí H2 ở đktc. Xác định công thức hóa học của oxit sắt trên. C©u 4(2,0®) Cho 5,4 gam Al vào dung dịch chứa 25,55 gam HCl, sau khi phản ứng kết thúc thu được V lít H2 ở đktc. Sau phản ứng chất nào dư? Khối lượng dư là bao nhiêu? Tính V. §¸p ¸n - biÓu ®iÓm Câu ý Đáp án Điểm 1 Mỗi đáp án đúng 0,25 điểm 3,0 Câu 1 2 3 4 5 6 7 8 9 10 11 Đ án A A D C B B C A D C B D 2 3,0 1. 4P + 5O2 2P2O5 2. 2Al + 3H2SO4 ® Al2(SO4)3 + 3H2 3. 2KMnO4 K2MnO4 + MnO2 + O2 4. FexOy + (y – x)CO xFeO + (y –x)CO2 5. 8Al + 3Fe3O4 4Al2O3 + 9Fe Phản ứng thế là: 2,5 0,5 0,5 0,5 0,5 0,5 0,5 3 2,0 1 nH= mH = 0,4 . 2 = 0,8(gam) m = 28,4 + mHO - mH = 28,4 + 7,2 – 0,8 = 34,8(gam) 0,5 0,5 2 nH= PTHH: FexOy + yH2 xFe + yH2O (1) Fe + 2HCl -> FeCl2 + H2 (2) Theo pt(2): nFe = nH= 0,3(mol) Theo pt (1): nO = nH= 0,4 (mol) => x : y = 0,3 : 0,4 = 3 : 4. Vậy CTHH: Fe3O4 0,5 0,5 4 2,0 1 1,0 nAl = ; nHCl = PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2 Ta có: . Vậy HCl dư, các chất tính theo Al. Theo pt: nHCl = 3nAl = 3 . 0,2 = 0,6(mol) nHCl(dư) = 0,7 – 0,6 = 0,1(mol) mHCl(dư) = 0,1 . 36,5 = 3,65(g) 0,25 0,25 0,25 0,25 2 1,0 Theo pt: nH= V = VH = 0,3 . 22,4 = 6,72(lít) 0,5 0,5
Tài liệu đính kèm:
 TUAN 26 - TIET52.doc
TUAN 26 - TIET52.doc





