Đề thi olympic môn Hóa học - Lớp 10 năm học: 2008 – 2009
Bạn đang xem tài liệu "Đề thi olympic môn Hóa học - Lớp 10 năm học: 2008 – 2009", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
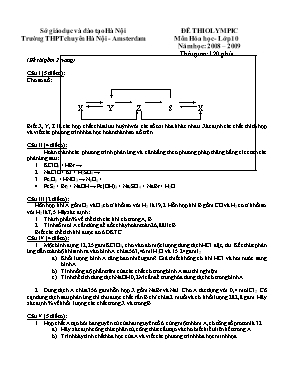
Sở giỏo dục và đào tạo Hà Nội Trường THPT chuyờn Hà Nội - Amsterdam ĐỀ THI OLYMPIC Mụn Húa học - Lớp 10 Năm học: 2008 – 2009 Thời gian: 120 phỳt (Đề thi gồm 2 trang) Cõu I (5 điểm): Cho sơ đồ: X Y Z S X Biết X, Y, Z là cỏc hợp chất chứa lưu huỳnh với cỏc số oxi húa khỏc nhau. Xỏc định cỏc chất thớch hợp và viết cỏc phương trỡnh húa học hoàn thành sơ đồ trờn. Cõu II (4 điểm): Hoàn thành cỏc phương trỡnh phản ứng và cõn bằng theo phương phỏp thăng bằng electron cỏc phản ứng sau: KClO3 + HBr đ NaClO + KI + H2SO4 đ FexOy + HNO3 đ NpOq + FeS2 + Br2 + NaOH đ Fe(OH)3 + Na2SO4 + NaBr + H2O Cõu III (2 điểm): Hỗn hợp khớ A gồm O2 và O3 cú tỉ khối so với H2 là 19,2. Hỗn hợp khớ B gồm CO và H2 co tỉ khối so với H2 là 7,5.Hóy xỏc định: Thành phần % về thể tớch cỏc khớ cú trong A, B. Tớnh số mol A cần dựng để đốt chỏy hoàn toàn 26,88 lớt B. Biết cỏc thể tớch khớ được đo ở ĐKTC. Cõu IV (4 điểm): Một bỡnh đựng 12,25 gam KClO3, cho vào đú một lượng dung dịch HCl đặc, dư. Kết thỳc phản ứng dẫn toàn bộ khớ sinh ra vào bỡnh A chứa 563,46 ml H2O và 15.24 gam I2. Khối lượng bỡnh A tăng bao nhiờu gam? Giả thiết khụng cú khớ HCl và hơi nước sang bỡnh A. Tớnh nồng độ phần trăm của cỏc chất cú trong bỡnh A sau thớ nghiệm. Tớnh thể tớch dung dịch NaOH 0,2M cần để trung hũa dung dịch cú trong bỡnh A. Dung dịch A chứa 356 gam hỗn hợp X gồm NaBr và NaI. Cho A tỏc dụng với 0,4 mol Cl2. Cụ cạn dung dịch sau phản ứng thỡ thu được chất rắn B chỉ chứa 2 muối và cú khối lượng 282,8 gam. Hóy xỏc định % về khối lượng cỏc chất trong X và trong B. Cõu V (5 điểm): Hợp chất A tạo bởi ba nguyờn tử của hai nguyờn tố ở cựng một nhúm A, cú tổng số proton là 32. Hóy xỏc định cụng thức phõn tử, cụng thức cấu tạo và cho biết kiểu liờn kết trong A. Trỡnh bày tớnh chất húa học của A và viết cỏc phương trỡnh húa học minh họa. Oxi húa 12,6 gam Fe bằng oxi thu được 17,4 gam hỗn hợp chất rắn A (gồm 4 chất). Hũa tan hoàn toàn A bằng dung dịch H2SO4 đặc núng, dư được V lớt khớ SO2 (đktc). Viết cỏc phương trỡnh húa học xảy ra. Tớnh V. Xỏc định thể tớch dung dịch H2SO4 98% (d = 1,84 g/ml) tối thiểu đó tham gia phản ứng. -------------------------------------------------------- Biết H = 1; C = 12; O = 16; S = 32; Cl = 35,5; Br = 80; I = 127; Na = 23; K = 39; Fe = 56; Ba = 137;Mn = 55 ĐÁP ÁN OLYMPIC LỚP 10 KHễNG CHUYấN Năm học 2008-2009 Đỏp ỏn Điểm Cõu I Chọn đỳng chất (VD: X-H2SO4 ; Y-H2S ; Z-SO2 ; ) Viết 9 phương trỡnh: 9 x 0,5 = Chỳ ý: - Bị tắc ở một phương trỡnh nào đú coi như sai hết - Thiếu điều kiện hoặc khụng cõn bằng trừ 0,25đ của pt - Viết sai sản phẩm: khụng tớnh điểm pt 5 đ 0,5đ 4,5đ Cõu II Mỗi pt 1đ: 1/ KClO3 + 6HBr đ 3Br2 + KCl + 3H2O 2/ NaClO + 2KI + H2SO4 đ I2 + NaCl + K2SO4 + H2O 3/ (5p-2q)FexOy + (18p-8q)xHNO3 đ (3x-2y)NpOq + (5p-2q)xFe(NO3)3 + (9p-q)xH2O 4/ 2FeS2 + 15Br2 + 38NaOH đ 2Fe(OH)3 + 4Na2SO4 + 30NaBr + 26H2O 4 đ Cõu III 1/ Trong hỗn hợp A, gọi số mol O2 là x và số mol O3 là y Trong hỗn hợp B, gọi số mol CO là a và số mol H2 là b 2/ nB = 1,2 mol (0,6 mol CO và 0,6 mol H2) CO + ẵ O2 đ CO2 ; CO + 1/3O3 đ CO2 H2 + ẵ O2 đ H2O ; H2 + 1/3O3 đ H2O C+2 đ C+4 + 2e ; H20 đ 2H+ + 2e 0,6 1,2 0,6 1,2 đ ồne (cho) = 2,4 mol Giả sử cú x mol hỗn hợp A (0,6x mol O2 và 0,4x mol O3) O2 + 4e đ 2O-2 ; O3 + 6e đ 3O-2 0,6x 2,4x 0,4x 2,4x đ ồne (nhận) = 4,8x đ x = 0,5 = nA 2đ 0,5đ 0,5đ 0,5đ 0,5đ Cõu IV 1/ = 0,1 mol ; = 0,06 mol KClO3 + 6HCl đ KCl + 3Cl2 + 3H2O 0,1 0,3 5Cl2 + I2 + 6H2O đ 2HIO3 + 10HCl 0,3 0,06 0,12 0,6 a. khối lượng bỡnh A tăng = mClo = 21,3 gam b. Bỡnh A gồm HIO3 : 0,12 mol (21,12 gam) HCl : 0,6 mol (21,9 gam) mdd A = 600 gam đ C% (HIO3) = 3,52% ; C% (HCl) = 3,65% c. HIO3 + NaOH đ NaIO3 + H2O HCl + NaOH đ NaCl + H2O nNaOH = + nHCl = 0,72 mol đ Vdd NaOH = 3,6 lớt 2/ Tớnh khử của I- mạnh hơn Br- đ thứ tự phản ứng Cl2 + 2NaI đ 2NaCl + I2 0,5x x x Khối lương giảm m = mNaI – mNaCl = 150x – 58,5x = 73,2 đ x = 0,8 p/ư= 0,5x = 0,4 = ban đầu đ NaBr chưa phản ứng Theo giả thiết: dung dịch sau phản ứng chỉ chứa 2 muối đ NaI phản ứng hết nNaI = 0,8 đ X gồm NaI: 120 gam (33,67%) và NaBr: 236 gam (66,34) B gồm NaCl 46,8 gam (16,55%) và NaBr 236 gam (83,45%) 4đ 0,25đ 0,5đ 0,25đ 0,5đ 0,5đ 1đ 0,5đ 0,5đ Cõu V 1/ Số p = Z, = 32 : 3 = 10,67 đ cú 1 nguyờn tố cú số Z < 10 đ thuộc chu kỡ 2 và 1 nguyờn tố thuộc chu kỡ 3. Z < 10 C N O F Si P S Cl Theo giả thiết, 2 nguyờn tố ở hai chu kỡ liờn tiếp nờn chỉ cú thể là O (Z=8) và S (Z=16) đ SO2 CTCT : Liờn kết cộng húa trị phõn cực Tớnh chất húa học: - Tớnh oxit axit - Tớnh oxi húa, tớnh khử 2/ a. Xỏc định A và 7 PTHH PTHH gồm 3 pt tạo oxit đ A gồm Fe, FeO, Fe2O3, Fe3O4 Và 4 pt của cỏc oxit với H2SO4 đặc núng b. Fe đ Fe3+ + 3e 0,225 0,225 0,675 đ số mol Fe2(SO4)3 n = ẵ = 0,1125 mol đ = 3. =0,3375 mol mO = 17,4 – 12,6 = 4,8 gam đ nO = 0,3 mol O + 2e đ O2- ; S+6 + 2e đ S+4 0,3 0,6 x 2x x Theo định luật bảo toàn e: 0,675 = 0,6 + 2x đ x = 0,0375 = nSO2 đ VSO2 = 0,84 lớt Từ pthh đ = 0,3375 + 0,0375 = 0,375 mol. đ = 36,75 gam đ mdd = 37,5 gam đ Vdd = 20,38 ml 5đ 1đ 1đ 1đ 1đ 0,5đ
Tài liệu đính kèm:
 K10- 2009- DE THI OLYMPIC HOA 10 HA NOI AMS.doc
K10- 2009- DE THI OLYMPIC HOA 10 HA NOI AMS.doc





