Đề kiểm tra học kỳ I năm học 2014 - 2015 môn: Hóa học 8 - Trường THCS Hòa Bình
Bạn đang xem tài liệu "Đề kiểm tra học kỳ I năm học 2014 - 2015 môn: Hóa học 8 - Trường THCS Hòa Bình", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
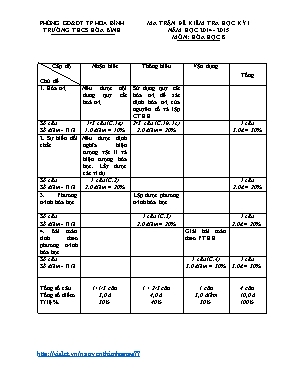
PHÒNG GD&ĐT TP HOA BÌNH TRƯỜNG THCS HÒA BÌNH MA TRẬN ĐỀ KIỂM TRA HỌC KỲ I NĂM HỌC 2014 - 2015 MÔN: HÓA HỌC 8 Cấp độ Chủ đề Nhận biết Thông hiểu Vận dụng Tổng 1. Hóa trị Nêu được nội dung quy tắc hoá trị Sử dụng quy tắc hóa trị để xác định hóa trị của nguyên tố và lập CTHH Số câu Số điểm - Tỉ lệ 1/3 câu (C.1a) 1,0 điểm = 10% 2/3 câu (C.1b, 1c) 2,0 điểm = 20% 1 câu 3,0đ = 30% 2. Sự biến đổi chất Nêu được định nghĩa hiện tượng vật lí và hiện tượng hóa học. Lấy được các ví dụ Số câu Số điểm - Tỉ lệ 1 câu (C.2) 2,0 điểm = 20% 1 câu 2,0đ = 20% 3. Phương trình hóa học Lập được phương trình hóa học Số câu Số điểm - Tỉ lệ 1 câu (C.3) 2,0 điểm = 20% 1 câu 2,0đ = 20% 4. Bài toán tính theo phương trình hóa học Giải bài toán theo PTHH Số câu Số điểm - Tỉ lệ 1 câu (C.4) 3,0 điểm = 30% 1 câu 3,0đ = 30% Tổng số câu Tổng số điểm Tỉ lệ % 1+1/3 câu 3,0 đ 30% 1 + 2/3 câu 4,0 đ 40% 1 câu 3,0 điểm 30% 4 câu 10,0 đ 100% PHÒNG GD&ĐT TP HÒA BÌNH TRƯỜNG THCS HÒA BÌNH ĐỀ KIỂM TRA HỌC KỲ I NĂM HỌC 2014 - 2015 MÔN: HÓA HỌC 8 Ngày kiểm tra: 26/12/2014 (Thời gian 45 phút, không kể thời gian giao đề) Câu 1: (3,0 điểm) a. Nêu quy tắc hoá trị và viết biểu thức tổng quát. b. Tính hoá trị của Zn trong hợp chất Zn(OH)2. Biết rằng nhóm (-OH) có hoá trị là I. c. Lập công thức hóa học của hợp chất tạo bởi Natri (Na) hóa tri (I) và oxi ( II) Câu 2: (2,0 điểm) Thế nào là hiện tượng vật lí, hiện tượng hóa học?. Mỗi loại hiện tượng lấy 2 ví dụ. Câu 3: (2,0 điểm) Hoàn thành sơ đồ phản ứng sau: a. H2 + O2 H2O b. Al + O2 Al2O3 c. Ca + H2O ------- Ca(OH)2 + H2 d. Fe(OH)3 Fe2O3 + H2O Câu 4: (3,0 điểm) Cho sơ đồ phản ứng sau: Zn + O2 ZnO Đốt cháy hết 13 gam Zn. a. Lập phương trình phản ứng cho sơ đồ trên. b. Tính thể tích khí oxi (ở điều kiện tiêu chuẩn) cần dùng. c. Tính khối lượng muối kẽm oxit taọ thành. (Biết Zn = 65; O = 16) .......................Hết........................... PHÒNG GD&ĐT TP HÒA BÌNH TRƯỜNG THCS HÒA BÌNH HƯỚNG DẪN CHẤM ĐỀ KIỂM TRA HỌC KỲ I NĂM HỌC 2014 - 2015 MÔN: HÓA HỌC 8 Câu Đáp án Điểm 1 (3,0đ) a. Quy tắc hóa trị: Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia. Công thức chung: AaxBby b. Gọi hóa trị của Zn trong hợp chất Zn(OH)2 là a. Theo quy tắc hóa trị, ta có: = 2 a = II. Vậy hóa trị của Zn trong hợp chất Zn(OH)2 là II c. Gọi công thức dạng chung NaxOy Áp dụng quy tắc hoá trị: x .I = y. II Hay : x/ y = II/ I= 1/2 => x = 2; y = 1 Vậy công thức cần tìm là Na2O 0,5 0,5 0,25 0,5 0,25 0,25 0,25 0,25 0,25 2 (2,0đ) - Hiện tượng chất biến đổi mà vẫn giữ nguyên là chất ban đầu được gọi là hiện tượng vật lí. VD1: ......; VD2.... - Hiện tượng chất biến đổi có tạo ra chất khác, được gọi là hiện tượng hóa học. VD1 .....; VD2..... 0,5 0,5 0,5 0,5 3 (2,0đ) a. 2H2 + O2 2H2O b. 4Al + 3O2 2Al2O3 c. Ca + 2H2O ------- Ca(OH)2 + H2 d. 2Fe (OH)3 Fe2O3 + 3H2O 0,5 0,5 0,5 0,5 4 (3,0đ) a. Phương trình hóa học: 2Zn + O2 2ZnO Số mol của Zn tham gia phản ứng là: nZn = (mol) b. Theo phương trình hóa học, ta thấy: n O= nZn = 0,2 = 0,1 (mol) Thể tích (ở đktc) khí oxi cần dùng cho phản ứng trên là: VO= n O 22,4 = 0,1 22,4 = 2,24 (l) c. Theo phương trình hóa học, ta thấy: nZn O = nZn = 0,2 (mol) Khối lượng kẽm oxit tạo thành là: mZnO = n ZnO 81 = 0,2 81 = 16,2 (g) 0,5 0,5 0,5 0,5 0,5 0,5
Tài liệu đính kèm:
 Kiểm tra HK1 Hóa 8 Hòa Bình1415.doc
Kiểm tra HK1 Hóa 8 Hòa Bình1415.doc





