Ma trận đề kiểm tra học kì I môn Hoá 8 – năm học: 2016 - 2017 - Trường THCS Huỳnh Thúc Kháng
Bạn đang xem tài liệu "Ma trận đề kiểm tra học kì I môn Hoá 8 – năm học: 2016 - 2017 - Trường THCS Huỳnh Thúc Kháng", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
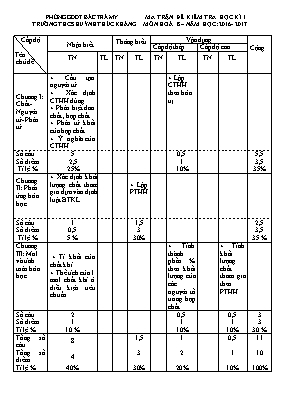
PHềNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG MA TRẬN ĐỀ KIỂM TRA HỌC Kè I MễN HOÁ 8 – NĂM HỌC: 2016- 2017 Cấp độ Tờn chủ đề Nhận biết Thụng hiểu Vận dụng Cộng Cấp độ thấp Cấp độ cao TN TL TN TL TN TL TN TL Chương I: Chất- Nguyờn tử- Phõn tử + Cấu tạo nguyờn tử. + Xỏc định CTHH đỳng. + Phõn biệt đơn chất , hợp chất. + Phõn tử khối của hợp chất. + í nghĩa của CTHH. + Lập CTHH theo húa trị. Số cõu 5 0,5 5,5 Số điểm Tỉ lệ % 2,5 25% 1 10% 3,5 35% Chương II: Phản ứng húa học + Xỏc định khối lượng chất tham gia dựa vào định luật BTKL. + Lập PTHH Số cõu Số điểm Tỉ lệ % 1 0,5 5 % 1,5 3 30% 2,5 3,5 35 % Chương III: Mol và tớnh toỏn húa học. + Tỉ khối của chất khớ. + Thể tớch của 1 mol chất khớ ở điều kiện tiờu chuẩn. + Tớnh thành phần % theo khối lượng của cỏc nguyờn tố trong hợp chất. + Tớnh khối lượng chất tham gia theo PTHH. Số cõu Số điểm Tỉ lệ % 2 1 10 % 0,5 1 10% 0,5 1 10% 3 3 30 % Tổng số cõu 8 1,5 1 0,5 11 Tổng số điểm 4 3 2 1 10 Tỉ lệ % 40% 30% 20% 10% 100% PHềNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG Họ và tờn:..................................................... Lớp:..................... ĐỀ KIỂM TRA HỌC KỲ I Năm học : 2016 - 2017 Mụn : Húa Học 8 Thời gian : 45 phỳt (khụng kể thời gian phỏt đề) Điểm: Lời phờ của giỏo viờn: I. Trắc nghiệm: (4 điểm) Khoanh trũn vào đỏp ỏn đỳng. Cõu 1: Hạt nhõn nguyờn tử được tạo bởi: A. Hạt proton và hạt electron C. Hạt proton và hạt nơtron B. Hạt nơtron và hạt electron D. Hạt proton, hạt nơtron và hạt electron Cõu 2: Một mol của bất kỡ chất khớ nào, trong cựng điều kiện về nhiệt độ và ỏp suất, đều chiếm những thể tớch bằng nhau và bằng : A. 224 lit B. 2,24 lit C. 22,4 lit D. 22,4 mili lit Cõu 3 : Tỉ khối của khớ O2 đối với khớ H2 bằng: A. 17 B. 16 C. 19 D. 20 Cõu 4: Dóy gồm cỏc hợp chất là: A. NO2, H2O, KOH, H3PO4 B. CO2, H2O, CO, Fe2O3 C. Fe, Cl2, C, N2 D. S, H2, Cl2, CO Cõu 5: Đốt chỏy 12,8 gam Đồng (Cu) trong bỡnh chứa Oxi (O2) thu được 16 gam Đồng(II) oxit (CuO). Khối lượng của oxi đó tham gia phản ứng chỏy là: A. 3,2 gam B. 4,8 gam C. 6,4 gam D. 1,67 gam Cõu 6: Từ cụng thức húa học K2CO3, hóy cho biết ý nào đỳng. Hợp chất trờn do 3 chất là K, C, O tạo nờn Hợp chất trờn do 3 nguyờn tố là K, C, O tạo nờn Hợp chất trờn do 3 nguyờn tử là K, C, O tạo nờn Hợp chất trờn do 3 phõn tử là K, C, O tạo nờn Cõu 7: Cỏc cụng thức húa học sau, cụng thức nào viết đỳng? A. Ca2O B. CaO C. SO2 D. NaCl2 Cõu 8 : Phõn tử khối của CaCO3 là: A. 96 (g) B. 98 (đvc) C. 100 (đvc) D. 100 (g) II/ TỰ LUẬN: (6 điểm ) Câu 1 (2,5 điểm): Lập phương trỡnh húa học của cỏc phản ứng sau: a/ Na2O + H2O ---> NaOH b/ Al2O3 + H2SO4 ---> Al2(SO4)3 + H2O c/ Zn + HCl ---> ZnCl2 + H2↑ d) NaOH + H2SO4 ----> Na2SO4 + H2O e/ N2O5 + H2O ----> HNO3 Cõu 2 ( 2 điểm): a/ Lập CTHH của Al (III) với SO4 (II) . b/ Tớnh thành phần phần trăm về khối lượng của mỗi nguyờn tố trong hợp chất Fe(OH)3. Cõu 3 (1,5 điểm): Cho 13 gam Kẽm tỏc dụng vừa đủ với axit clohiđric theo phương trỡnh: Zn + HCl ----> ZnCl2 + H2 a) Lập phương trỡnh húa học của phản ứng trờn? b) Tớnh khối lượng axit clohiđric (HCl) đó dựng ? (Cho KLNT: Zn = 65; H = 1; Cl = 35,5) - HẾT- Phờ duyệt của tổ trưởng Người ra đề Huỳnh Thị Thu Hiền PHềNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG KIỂM TRA HỌC Kè I Năm học : 2016 - 2017 Mụn : Húa Học 8 ĐÁP ÁN VÀ BIỂU ĐIỂM: I. Trắc nghiệm: (4 điểm) mỗi cõu trả lời đỳng được 0,5 điểm Cõu 1 2 3 4 5 6 7 8 Đỏp ỏn C C B A, B A B B, C C II II. Tự luận: ( 6 điểm) Cõu Đỏp ỏn Thang điểm 1 (2,5 điểm) a/ Na2O + H2O → 2 NaOH b/ Al2O3 + 3 H2SO4 → Al2(SO4)3 + 3 H2O c/ Zn + 2 HCl → ZnCl2 + H2↑ d) 2 NaOH + H2SO4 → Na2SO4 + 2 H2O e/ N2O5 + H2O → 2 HNO3 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm 2 (2 điểm) a) III II Alx(SO4) y Theo quy tắc húa trị, ta cú: x*III = y*II = = x = 2 và y = 3 Vậy CTHH là Al2(SO4)3 b)Ta cú: M = 56+(16+1)*3 = 107 (g/mol) %Fe = 100% = 52,34 (%) ; %O = 100% = 44,86 (%) ; %H = 100% = 2,80 (%) 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 0,25 điểm 3(1,5 điểm) a, Phương trỡnh húa học: Zn + 2HCl ZnCl2 + H2 1 mol 2 mol b, mZn = 13 (g) =>nHCl = 13/65=0.2 mol Theo phương trỡnh ta cú: nHCl = 2 nZn = 2. 0,2 = 0.4 mol mHCl = nHCl . MHCl = 0.4. 36,5 = 14.6 g Vậy khối lượng của HCl đú dựng là 14.6g 0,5 điểm 0,25 điểm 0,25 điểm 0,5 điểm ĐỀ DÀNH CHO HỌC SINH KHUYẾT TẬT PHềNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG Họ và tờn:..................................................... Lớp:..................... ĐỀ KIỂM TRA HỌC KỲ I Năm học : 2016 - 2017 Mụn : Húa Học 8 Thời gian : 45 phỳt (khụng kể thời gian phỏt đề) Điểm: Lời phờ của giỏo viờn: I. Trắc nghiệm: (8 điểm) Khoanh trũn vào đỏp ỏn đỳng. Cõu 1: Hạt nhõn nguyờn tử được tạo bởi: A. Hạt proton và hạt electron C. Hạt proton và hạt nơtron B. Hạt nơtron và hạt electron D. Hạt proton, hạt nơtron và hạt electron Cõu 2: Một mol của bất kỡ chất khớ nào, trong cựng điều kiện về nhiệt độ và ỏp suất, đều chiếm những thể tớch bằng nhau và bằng : A. 224 lit B. 2,24 lit C. 22,4 lit D. 22,4 mili lit Cõu 3 : Tỉ khối của khớ O2 đối với khớ H2 bằng: A. 17 B. 16 C. 19 D. 20 Cõu 4: Dóy gồm cỏc hợp chất là: A. NO2, H2O, KOH, H3PO4 B. CO2, H2O, CO, Fe2O3 C. Fe, Cl2, C, N2 D. S, H2, Cl2, CO Cõu 5: Đốt chỏy 12,8 gam Đồng (Cu) trong bỡnh chứa Oxi (O2) thu được 16 gam Đồng(II) oxit (CuO). Khối lượng của oxi đó tham gia phản ứng chỏy là: A. 3,2 gam B. 4,8 gam C. 6,4 gam D. 1,67 gam Cõu 6: Từ cụng thức húa học K2CO3, hóy cho biết ý nào đỳng. Hợp chất trờn do 3 chất là K, C, O tạo nờn Hợp chất trờn do 3 nguyờn tố là K, C, O tạo nờn Hợp chất trờn do 3 nguyờn tử là K, C, O tạo nờn Hợp chất trờn do 3 phõn tử là K, C, O tạo nờn Cõu 7: Cỏc cụng thức húa học sau, cụng thức nào viết đỳng? A. Ca2O B. CaO C. SO2 D. NaCl2 Cõu 8 : Phõn tử khối của CaCO3 là: A. 96 (g) B. 98 (đvc) C. 100 (đvc) D. 100 (g) II/ TỰ LUẬN: (2 điểm ) Lập phương trỡnh húa học của cỏc phản ứng sau: a/ Na2O + H2O ---> NaOH b/ Zn + HCl ---> ZnCl2 + H2↑ c) NaOH + H2SO4 ----> Na2SO4 + H2O d/ N2O5 + H2O ----> HNO3 - HẾT- Phờ duyệt của tổ trưởng Người ra đề Huỳnh Thị Thu Hiền ĐÁP ÁN ĐỀ DÀNH CHO HỌC SINH KHUYẾT TẬT PHềNG GDĐT BẮC TRÀ MY TRƯỜNG THCS HUỲNH THÚC KHÁNG KIỂM TRA HỌC Kè I Năm học : 2016 - 2017 Mụn : Húa Học 8 ĐÁP ÁN VÀ BIỂU ĐIỂM: I. Trắc nghiệm: (8 điểm) mỗi cõu trả lời đỳng được 1 điểm Cõu 1 2 3 4 5 6 7 8 Đỏp ỏn C C B A, B A B B, C C II II. Tự luận: ( 2 điểm) Đỏp ỏn Thang điểm a/ Na2O + H2O → 2 NaOH b/ Zn + 2 HCl → ZnCl2 + H2↑ c/ 2 NaOH + H2SO4 → Na2SO4 + 2 H2O d/ N2O5 + H2O → 2 HNO3 0,5 điểm 0,5 điểm 0,5 điểm 0,5 điểm
Tài liệu đính kèm:
 de_kiem_tra_hoc_ki_1.doc
de_kiem_tra_hoc_ki_1.doc





