Kiểm tra học kỳ I năm học 2016 - 2017 môn: Hóa học 9 - trường TH & THCS Kỳ Thượng
Bạn đang xem tài liệu "Kiểm tra học kỳ I năm học 2016 - 2017 môn: Hóa học 9 - trường TH & THCS Kỳ Thượng", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
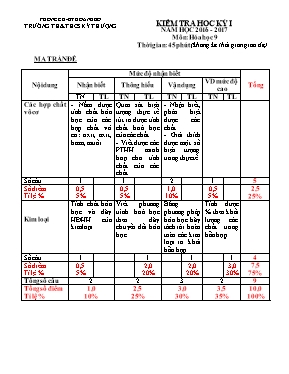
PHÒNG GD-ĐT HOÀNH BỒ TRƯỜNG TH&THCS KỲ THƯỢNG KIỂM TRA HỌC KỲ I NĂM HỌC 2016 - 2017 Môn: Hóa học 9 Thời gian: 45 phút (không kể thời gian giao đề) MA TRẬN ĐỀ Nội dung Mức độ nhận biết Tổng Nhận biết Thông hiểu Vận dụng VD mức độ cao TN TL TN TL TN TL TN TL Các hợp chất vô cơ - Nắm được tính chất hóa học của các hợp chất vô cơ: oxit, axit, bazơ, muối Quan sát hiện tượng thực tế rút ra được tính chất hoá học của các chất - Viết được các PTHH minh hoạ cho tính chất của các chất - Nhận biết, phân biệt được các chất - Giải thích được một số hiện tượng trong thực tế. Số câu 1 1 2 1 5 Số điểm Tỉ lệ % 0,5 5% 0,5 5% 1,0 10% 0,5 5% 2,5 25% Kim loại Tính chất hóa học và dãy HĐHH của kim loại. Viết phương trình hoá học theo dãy chuyển đổi hóa học Bằng phương pháp hóa học hãy tách rời hoàn toàn các kim loại ra khỏi hỗn hợp Tính được % theo khối lượng các chất trong hỗn hợp. Số câu 1 1 1 1 4 Số điểm Tỉ lệ % 0,5 5% 2,0 20% 2,0 20% 3,0 30% 7,5 75% Tổng số câu 2 2 3 2 9 Tống số điểm Tỉ lệ % 1,0 10% 2,5 25% 3,0 30% 3,5 35% 10,0 100% PHÒNG GD-ĐT HOÀNH BỒ TRƯỜNG TH&THCS KỲ THƯỢNG KIỂM TRA HỌC KỲ I NĂM HỌC 2016 - 2017 Môn: Hóa học 9 Thời gian: 45 phút (không kể thời gian giao đề) ĐỀ BÀI I. Phần trắc nghiệm: (3đ) Chọn phương án đúng cho các câu sau: Câu 1: Để loại khí CO2 có lẫn trong khí O2, người ta sục hỗn hợp đi qua dung dịch: A. HCl dư B. Ca(OH)2 dư C. NaCl dư D. Na2SO4 dư Câu 2 : Để nhận biết các dd H2SO4, KOH, K2SO4 có thể dung thuốc thử nào sau đây : A. dd phenolphtalein C. dd BaCl2 B. Quỳ tím D. dd Ba(NO3)2 Câu 3 : Thí nghiệm nào sau đây tạo kết tủa khi trộn? A. dd HCl và dd NaOH C. Kim loại Al và dd H2SO4 B. dd NaCl và dd BaSO4 D. dd BaCl2 và dd Na2SO4 Câu 4: Phân đạm nào sau đây có phần trăm nitơ cao nhất: A. Ure (CO(NH2)2) C. Amoni sunfat ((NH4)2SO4) B. Amoni nitrat (NH4NO3) D. Kali nitrat (KNO3) Câu 5: Một bình hở miệng đựng dd Ca(OH)2 để lâu ngày trong không khí (bỏ qua lượng nước bay hơi) thì khối lượng bình thay đổi như thế nào? A. Không thay đổi C. Tăng lên B. Giảm đi D. Tăng lên rồi giảm đi Câu 6: Dung dịch ZnCl2 có lẫn tạp chất là CuCl2. Dùng kim loại nào sau đây để làm sạch dung dịch ZnCl2: A. Fe B. Zn C. Cu D. Al II, Phần tự luận: Câu 1 ( 2 điểm): Viết phương trình hoá học theo dãy chuyển đổi hóa học sau: (ghi rõ điều kiện phản ứng – nếu có) FeS2 → Fe2O3 → Fe2(SO4)3 → FeCl3 → Fe(OH)3 Câu 2 ( 2 điểm): Một hỗn hợp gồm Al, Cu và Ag. Bằng phương pháp hóa học hãy tách rời hoàn toàn các kim loại ra khỏi hỗn hợp trên. Viết phương trình hoá học xảy ra. Câu 3 ( 3 điểm): Hòa tan hoàn toàn 20 gam hỗn hợp Fe và Cu trong dung dịch HCl dư, phản ứng xong thu được 4,48 lít khí hiđro (đktc). Tính phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp. (Biết Fe = 56, Cu = 64, O = 16, H =1) HƯỚNG DẪN CHẤM BÀI Phần Câu Đáp án Biểu điểm Trắc nghiệm (3đ) 1 B 0,5 2 B 0,5 3 D 0,5 4 A 0,5 5 C 0,5 6 B 0,5 Tự luận (7đ) 1 (2đ) (1): 4FeS + 11O2 → 2Fe2O3 + 8SO2 (2): Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O (3): Fe2(SO4)3 + 3BaCl2 → 2FeCl3 + 3BaSO4↓ (4): FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl 0,5 0,5 0,5 0,5 2 (3đ) Cho hỗn hợp phản ứng với dung dịch kiềm chỉ có Al tan do phản ứng: 2Al + 2NaOH + H2O → 2NaAlO2 + 3H2 Lọc tách Fe và Cu. Phần nước lọc thu được cho phản ứng với dung dịch HCl vừa đủ sẽ sinh ra kết tủa keo trắng: 2NaAlO2 + HCl + H2O → Al(OH)3↓ + NaCl Lọc kết tủa rồi nung với H2 trong điều kiện nhiệt độ cao ta sẽ thu được Al tº 2Al(OH)3 + 3H2 →2Al + 6H2O Hỗn hợp Fe và Cu cho phản ứng với dung dịch HCl chỉ có Fe phản ứng Fe + HCl → FeCl2 + H2 Lọc thu được Cu. Phần nước lọc thu được cho phản ứng với dung dịch kiềm sẽ cho kết tủa trắng xanh FeCl2 + 2NaOH → Fe(OH)2↓+ 2NaCl Lọc kết tủa nung nóng với H2 ở nhiệt độ cao ta thu được Fe: tº Fe(OH)2 + H2 → Fe +2H2O 0,5 0,25 0,25 0,25 0,25 0,25 0,25 3 (3đ) Theo bài ra ta có: nH= = 0,2 (mol) - PTHH: Fe + 2HCl FeCl2 + H2 0,2(mol) 0,2(mol) Khối lượng của đồng: 20 – (0,2 56) = 8,8 (gam) % Cu = % Fe = 100% - 44% = 56% Ghi chú: Không cân bằng số phân tử HCl, tính đúng, ghi ½ tổng điểm toàn bài. 0,5 1,0 0,5 0,5 0,5 ( Nếu HS có cách giải khác đúng bản chất hóa học vẫn cho điểm tối đa)
Tài liệu đính kèm:
 De_thi_va_dap_an_Hoa_hoc_9_HKI_co_ma_tran.doc
De_thi_va_dap_an_Hoa_hoc_9_HKI_co_ma_tran.doc





