Kiểm tra học kỳ I năm học 2016 - 2017 môn: Hóa học 8 - Trường TH & THCS Kỳ Phượng
Bạn đang xem tài liệu "Kiểm tra học kỳ I năm học 2016 - 2017 môn: Hóa học 8 - Trường TH & THCS Kỳ Phượng", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
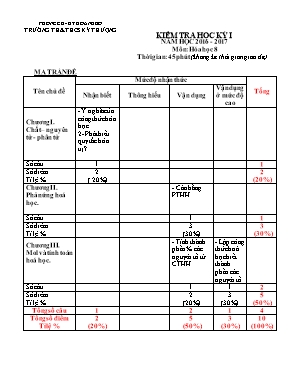
PHÒNG GD - ĐT HOÀNH BỒ TRƯỜNG TH&THCS KỲ THƯỢNG KIỂM TRA HỌC KỲ I NĂM HỌC 2016 - 2017 Môn: Hóa học 8 Thời gian: 45 phút (không kể thời gian giao đề) MA TRẬN ĐỀ Tên chủ đề Mức độ nhận thức Tổng Nhận biết Thông hiểu Vận dụng Vận dụng ở mức độ cao Chương I. Chất – nguyên tử - phân tử - Ý nghĩa của công thức hóa học 2- Phát biểu quy tắc hóa trị? Số câu 1 1 Số điểm Tỉ lệ % 2 ( 20%) 2 (20%) Chương II. Phản ứng hoá học. - Cân bằng PTHH Số câu 1 1 Số điểm Tỉ lệ % 3 (30%) 3 (30%) Chương III. Mol và tính toán hoá học. - Tính thành phần % các nguyên tố từ CTHH - Lập công thức hoá học biết thành phần các nguyên tố. Số câu 1 1 2 Số điểm Tỉ lệ % 2 (20%) 3 (30%) 5 (50%) Tổng số câu 1 2 1 4 Tổng số điểm Tỉ lệ % 2 (20%) 5 (50%) 3 (30%) 10 (100%) PHÒNG GD - ĐT HOÀNH BỒ TRƯỜNG TH&THCS KỲ THƯỢNG KIỂM TRA HỌC KỲ I NĂM HỌC 2016 - 2017 Môn: Hóa học 8 Thời gian: 45 phút (không kể thời gian giao đề) ĐỀ BÀI: Câu 1: ( 2 điểm ) 1- Cho công thức hóa học sau: HNO3 Cho biết ý nghĩa của công thức hóa học trên. 2- Phát biểu quy tắc hóa trị? Vận dụng: Tính hóa trị của Mg trong hợp chất MgSO4 biết nhóm (SO4) có hóa trị II. Câu 2: ( 2 điểm): Cho CTHH sau: Ca(NO3)2 Tính thành phần % theo khối lượng các nguyên tố trong công thức hóa học trên. Câu 3( 3 điểm): Lập công thức hoá học hợp chất sau: a, Hợp chất A có khối lượng mol là 16g, thành phần các nguyên tố : 75%C ; 25%H b, Hợp chất khí B có thành phần % theo khối lượng là 82,35% N và 17,65% H. Tỉ khối của khí B so với Hiđro là 8,5. Câu 4( 3 điểm): Cân bằng PTHH theo các sơ đồ phản ứng sau: a, Zn + HCl → ZnCl2 + H2 b) BaCl2 + Al2(SO4)3 → BaSO4 + AlCl3 c) Fe + Cl2 FeCl3 d) Fe2O3 + H2 Fe + H2O e, FeCl3 + Ag2SO4 → Fe2(SO4)3 + AgCl f, Fe(OH)3 → Fe2O3 + H2O ---Hết--- HƯỚNG DẪN CHẤM Câu Đáp án Biểu điểm 1 1- Ý nghĩa của công thức hóa học HNO3 3 nguyên tố là H, N O. 1 nguyên tử H, 1 nguyên tử N và 3 nguyên tử O 63 đvC 2- Quy tắc hóa trị: Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia. - Hóa trị của Mg trong hợp chất MgSO4 : Gọi hóa trị của Mg là a, ta có: 1 x a = 1 x II => a = II 1.0 1.0 2 Cho CTHH sau: Ca(NO3)2 - M Ca(NO3)2 = 40 + (14 + 3.16).2 = 164 (g) - Trong 1 mol KNO3 có: - 1mol nguyên tử K vậy mCa = 40 (g) - 2mol nguyên tử N vậy mN = 28 (g) - 6mol nguyên tử O vậy mO = 16. 6 = 96 (g) 40. 100% % Ca = = 24,39% 164 28 . 100% % N = = 17,07% 101 96. 100% % O = = 58,54% 101 (hoặc % O = 100% - (% K + % N) = 100% - (24,39% + 17,07%) 0,5 0.25 0.25 0.25 0.25 0.25 0.25 3 a, CTHH của A: CH4 b, CTHH của B: NH3 1,5 1,5 4 Cân bằng PTHH theo các sơ đồ phản ứng sau: a, Zn + 2HCl → ZnCl2 + H2 b, 3BaCl2 + Al2(SO4)3 → 3BaSO4 + 2AlCl3 tº c, 2Fe + 3Cl2 2FeCl3 tº d, Fe2O3 + 3H2 2Fe + 3H2O e, 2FeCl3 + 3Ag2SO4 → Fe2(SO4)3 + 6AgCl f, 2Fe(OH)3 → Fe2O3 + 3H2O 0.5 0.5 0.5 0.5 0.5 0.5 HS có cách giải khác đúng bản chất hóa học vẫn cho điểm tối đa
Tài liệu đính kèm:
 De_thi_va_dap_an_Hoa_hoc_8_HKI_co_ma_tran.doc
De_thi_va_dap_an_Hoa_hoc_8_HKI_co_ma_tran.doc





