Kiểm tra chất lượng học kì I năm học: 2015 – 2016 môn : Hóa học lớp 9 thời gian: 45 phút ( không kể thời gian giao đề)
Bạn đang xem tài liệu "Kiểm tra chất lượng học kì I năm học: 2015 – 2016 môn : Hóa học lớp 9 thời gian: 45 phút ( không kể thời gian giao đề)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
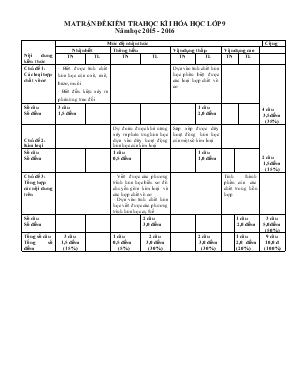
MA TRẬN ĐỀ KIỂM TRA HỌC KÌ I HĨA HỌC LỚP 9 Năm học 2015 - 2016 Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thơng hiểu Vận dụng thấp Vận dụng cao TN TL TN TL TN TL TN TL Chủ đề 1: Các loại hợp chất vơ cơ - Biết được tính chất hĩa học của oxit, axit, bazơ, muối - Biết điều kiện xảy ra phản ứng trao đổi Dựa vào tính chất hĩa học phân biệt được các loại hợp chất vơ cơ 4 câu 3,5 điểm (35%) Số câu Số điểm 3 câu 1,5 điểm 1 câu 2,0 điểm Chủ đề 2: Kim loại Dự đốn được khả năng xảy ra phản ứng hĩa học dựa vào dãy hoạt động hĩa học của kim loại Sắp xếp được dãy hoạt đơng hĩa học của một số kim loại 2 câu 1,5 điểm (15%) Số câu Số điểm 1 câu 0,5 điểm 1 câu 1,0 điểm Chủ đề 3: Tổng hợp các nội dung trên - Viết được các phương trình hĩa học biểu sơ đồ chuyển giữa kim loại và các hợp chất vơ cơ - Dựa vào tính chất hĩa học viết được các phương trình hĩa học cụ thể Tính thành phần của các chất trong hỗn hợp Số câu Số điểm 2 câu 3,0 điểm 1 câu 2,0 điểm 3 câu 5,0 điểm (50%) Tổng số câu Tổng số điểm 3 câu 1,5 điểm (15%) 1 câu 0,5 điểm (5%) 2 câu 3,0 điểm (30%) 2 câu 3,0 điểm (30%) 1 câu 2,0 điểm (20%) 9 câu 10,0 đ (100%) KIỂM TRA CHẤT LƯỢNG HỌC KÌ I Năm học: 2015 – 2016 Mơn : Hĩa học lớp 9 Thời gian: 45 phút( khơng kể thời gian giao đề) Phần I: Trắc nghiệm ( 2,0 điểm) Khoanh trịn vào chữ cái A, B, C hoặc D trước câu trả lời đúng nhất Câu 1: Cặp chất nào sau đây tác dụng với nhau tạo thành muối và nước? A. Mg và H2SO4 B. MgO và H2SO4 C. Mg(NO3)2 và NaOH D. MgCl2 và NaOH Câu 2: Cặp chất nào sau đây tác dụng với nhau tạo thành sản phẩm khí? A. BaO và HCl B. Ba(OH)2 và HCl C. BaCO3 và HCl D. BaCl2 và H2SO4 Câu 3: Trường hợp nào sau đây cĩ phản ứng tạo sản phẩm là chất kết tủa màu xanh? A. Cho Al vào dung dịch HCl B. Cho Zn vào dung dịch AgNO3 C. Cho dung dịch KOH vào dung dịch FeCl3 D. Cho dung dịch NaOH vào dung dịch CuSO4 Câu 4: Dùng dung dịch nào sau đây để làm sạch Ag cĩ lẫn Al, Fe, Cu ở dạng bột? A. H2SO4 lỗng B. FeCl3 C. CuSO4 D. AgNO3 Phần II: Tự luận ( 8,0 điểm) Câu 1: (1,0 điểm) Cĩ bốn kim loại: A, B, C, D đứng sau Mg trong dãy hoạt động hĩa học. Biết rằng: + A và B khơng phản ứng với dung dịch HCl + C và D tác dụng với dung dịch HCl giải phĩng khí hiđro. + A tác dụng với dung dịch muối của B và giải phĩng B. + D tác dụng với dung dịch muối của C và giải phĩng C. Hãy xác định thứ tự sắp xếp các kim loại trên theo chiều hoạt động hĩa học giảm dần. Câu 2: (2,0 điểm) Viết các phương trình hĩa học thực hiện dãy biến đổi hĩa học theo sơ đồ sau: Fe(NO3)3 Fe(OH)3 Fe2O3 Fe FeCl2 Câu 3: ( 2,0 điểm) Cĩ bốn dung dịch đựng trong bốn ống nghiệm riêng biệt là NaOH, HCl, NaNO3, NaCl. Hãy nêu phương pháp hĩa học để phân biệt bốn dung dịch này. Viết các phương trình hĩa học( nếu cĩ) để minh họa. Câu 4: ( 3,0 điểm) Cho 23,2 gam hỗn hợp Mg và Fe tác dụng với dung dịch HCl dư thu được 11,2 (l) H2 (đktc). Viết phương trình phản ứng. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu (Mg = 24; Fe = 56) ĐÁP ÁN VÀ BIỂU ĐIỂM Phần I: Trắc nghiệm ( 2,0 điểm) BIỂU ĐIỂM Câu 1 Câu 2 Câu 3 Câu 4 B C D D 0,5 x 4 = 2,0 điểm PHẦN II: Tự luận ( 8,0điểm) Câu 1 Từ các gợi ý của đề bài: + A và B xếp sau H + C và D xếp trước H + A xếp trước B + D xếp trước C Vậy: D, C, A, B ( Nếu học sinh chỉ ghi: D, C, A, B thì được 0,5 điểm) 1,0đ Câu 2 (1) Fe(NO3)3 + 3NaOH Fe(OH)3 + 3NaNO3 (2) 2Fe(OH)3 Fe2O3 + 3H2O (3) Fe2O3 + 3CO 2Fe + 3CO2 (4) Fe + 2HCl FeCl2 + H2 Học sinh sử dụng phương trình hĩa học khác đúng vẫn đạt điểm tối đa. Nếu viết được nhưng khơng cân bằng hoặc thiếu điều kiện thì được 0,25 điểm cho mỗi phương trình 0,5 đ 0,5 đ 0,5 đ 0,5 đ Câu 3 - Nhúng quì tím vào bốn ống nghiệm + Nếu quì tím chuyển thành màu xanh là NaOH + Nếu quì tím chuyển thành màu đỏ là HCl - Cho dung dịch AgNO3 vào hai ống nghiệm khơng làm đổi màu quì tím. + Ống nghiệm nào xuất hiện kết tủa trắng là NaCl + Ống nghiệm khơng cĩ hiện tượng là NaNO3 Phương trình: NaCl + AgNO3 NaNO3 + AgCl 0,25 đ 0,25 đ 0,25 đ 0,25 đ 0,25 đ 0,25 đ 0,5 đ Câu 4 a/ PTHH Mg + 2HCl MgCl2 + H2 (1) a mol a mol Fe + 2HCl FeCl2 + H2 (2) b mol b mol b/ Số mol của Khí H2: n = = 0,5 mol Theo (1) và (2), ta cĩ: a + b = 0,5 Theo đề bài: 24a + 56b = 23,2 Giải hệ phương trình, ta cĩ: a = 0,15; b = 0,35 mMg = 0,15 x 24 = 3,6 g mFe = 0,35 x 56 = 19,6 g ( Học sinh giải cách khác đúng vẫn đạt điểm tối đa) 0,5 đ 0,5 đ 0,5 đ 0,25 đ 0,25 đ 0,5 đ 0,5 đ Tổng 10,0đ
Tài liệu đính kèm:
 de_kiem_tra_hoa_9_HK1.doc
de_kiem_tra_hoa_9_HK1.doc





