Kiểm tra 45 phút (tiết 25) môn: Hóa học 8 - Trường THCS Hùng Tiến
Bạn đang xem tài liệu "Kiểm tra 45 phút (tiết 25) môn: Hóa học 8 - Trường THCS Hùng Tiến", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
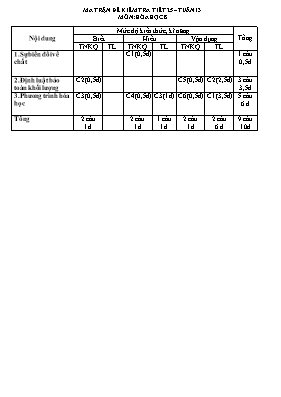
MA TRẬN ĐỀ KIỂM TRA TIẾT 25 – TUẦN 13 MÔN: HÓA HỌC 8 Nội dung Mức độ kiến thức , kĩ năng Tổng Biết Hiểu Vận dụng TNKQ TL TNKQ TL TNKQ TL 1.Sự biến đổi về chất C1(0,5đ) 1 câu 0,5đ 2. Định luật bảo toàn khối lượng C2(0,5đ) C5(0,5đ) C2(2,5đ) 3 câu 3,5đ 3.Phương trình hóa học C3(0,5đ) C4(0,5đ) C3(1đ) C6(0,5đ) C1(3,5đ) 5 câu 6 đ Tổng 2 câu 1đ 2 câu 1đ 1 câu 1đ 2 câu 1đ 2 câu 6 đ 9 câu 10đ Trường THCS Hùng tiến Họ và tên : LỚP : 8... Thứ ngày tháng năm 2015 KIỂM TRA 45 phút (Tiết 25) Môn : Hóa học 8 Điểm Nhận xét của thầy, cô giáo ĐỀ BÀI A. Phần trắc nghiệm khách quan: (3điểm) Em hãy khoanh tròn vào các đáp án em cho là đúng(mỗi câu 0.5điểm) Câu 1: Các hiện tượng dưới đây đâu là hiện tượng hóa học a. Hòa tan muối ăn vào nước được nước muối. b. Khi đánh diêm có lửa bắt cháy. c. Thanh đồng được kéo thành sợi nhỏ để làm dây điện. d. Thuỷ tinh được đun nóng chảy ở nhiệt độ cao rồi thổi thành bóng đèn, lọ hoa, cốc e. Cho 1 mẫu đá vôi vào giấm ăn thấy có bọt khí thóat ra. Câu 2: Phát biểu nào sau đây đúng? a. trong 1 PƯHH, tổng khối lượng các chất sản phẩm bằng tổng khối lượng các chất tham gia. b. trong 1 PƯHH, số nguyên tử của mỗi nguyên tố được bảo toàn. c. trong 1 PƯHH, số phân tử của các chất được bảo toàn d. trong 1 PƯHH có n chất nếu biết khối lượng của (n-1) chất thì tính được khối lượng của chất còn lại. Câu 3: Trong phản ứng hóa học, phân tử này biến đổi thành phân tử khác là do a. Các nguyên tử tác dụng với nhau. b. Các nguyên tố tác dụng với nhau. c. Liên kết giữa các nguyên tử thay đổi. d. Liên kết giữa các nguyên tử không bị thay đổi Câu 4:Cho sơ đồ phản ứng hóa học: Al + O2 ----> AlxOy Khi x ¹y thì x, y có thể lần lượt là: a. x = 2; y =1 b. x = 2; y =3 b. x = 1; y = 2 d. x = 3; y = 2 Câu 5: Cho 8,4 gam CO tác dụng với 16 gam Fe2O 3 tạo ra 13,2 gam CO2 và kim loại Fe. Khối lượng sắt thu được là: a. 2,24g b. 22,4g c. 11,2g d. 1,12g. Câu 6: Khí Nitơ và khí Hidro tác dụng với nhau tạo ra khí Amoniac (NH3). PTHH nào dưới đây viết đúng: a. N + 3H " NH3 b. N2 + H2 " NH3 c. N2 + H2 " 2NH3 d. N2 + 3H2 " 2NH3 Phần B: Tự luận (7 điểm) Câu 1 (3,5điểm): 1. Lập PTHH của các phản ứng sau a. Mg + HCl MgCl2 + H2 b. Fe2O3 + CO Fe + CO2 c. Al + H2SO4 Al2(SO4)3 + H2 d. Al + Cl2 AlCl3. e. Fe(OH)3 + H2SO4 ----> Fe2(SO4)3 + H2O f. M + HNO3 --- > M(NO3)n + H2 2. Cho biết tỉ lệ số nguyên tử, phân tử của cặp đơn chất và cặp hợp chất trong phản ứng câu c ? Câu 2 (2 điểm): Cho 8,4g bột sắt cháy hết trong 3,2g khí oxi (đktc) tạo ra oxit sắt từ (Fe3O4). a. Viết PTHH của phản ứng và cho biết tỉ lệ số nguyên tử, phân tử của các chất trong phản ứng. b. Tính khối lượng oxit sắt từ tạo thành. Câu 3 (1,5điểm) : Lập phương trình phản ứng sau đây? Dấu hiệu nào chứng tỏ rằng phản ứng đã xảy ra Phốt pho đỏ P cháy sáng sinh ra đi phốt pho pentaoxit P2O5 Magie tác dụng với axit sunfuric H2SO4 tạo ra Magie sunfat MgSO4 và khí hiđrô H2. Bài làm ..................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................... .................................................................................................................................................................... ..................................................................................................................................................................... ................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................ .................................................................................................................................................................... ..................................................................................................................................................................... Đáp án – biểu điểm Môn : Hóa Học 8 – tiết25 A - Phần trắc nghiệm :(3điểm) Câu 1 2 3 4 5 6 Đáp án B,e A,b,d C B C D II. Tự luận (6 điểm) Câu Đáp án Điểm Câu 1 (3,5 điểm) 1.a. Mg + 2HCl ® MgCl2 + H2 b. Fe2O3 + 3CO ® 2Fe + 3CO2 c. 2Al + 3H2SO4 ® Al2(SO4)3 + 3H2 d. 2Al + 3Cl2 ® 2AlCl3. e. 2Fe(OH)3 + 3 H2SO4 ® Fe2(SO4)3 + 6 H2O f. 2 M + 2nHNO3 --- > 2M(NO3)n + n H2 2. Tỉ lệ :Al: H2 = 2:3 H2SO4: Al2(SO4)3= 3:1 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ 0,5 đ Câu 2 (2 điểm) a. 3Fe + 2O2 ® Fe3O4 Số nguyên tử Fe : số nguyên tử O2 : số phân tử Fe3O4 = 3:2:1 b. Áp dụng ĐLBTKL ta có: ® = 8,4 + 3,2 = 11,6 g 0,5đ 0,5đ 0,5đ 0,5đ Câu 3 (1,5 điểm) a, PTHH: 4P + 5O2 ® 2P2O5 - dấu hiệu cháy sáng b, PTHH: Mg + H2SO4 ® MgSO4 + H2 - dấu hiệu có khí thoát ra khỏi dung dịch 0,5đ 0,25đ 0,5đ 0,25đ
Tài liệu đính kèm:
 ktra_hoa_8_t25_ko_can_chinh.doc
ktra_hoa_8_t25_ko_can_chinh.doc





