Giáo án Tuần 5 - Tiết 10 - Kiểm tra 45 phút môn hóa học 9
Bạn đang xem tài liệu "Giáo án Tuần 5 - Tiết 10 - Kiểm tra 45 phút môn hóa học 9", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
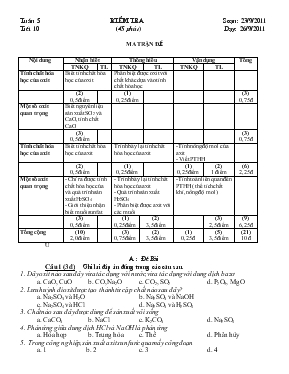
TuÇn 5 kiÓm tra So¹n: 23/9/2011 TiÕt 10 (45 phót) D¹y: 26/9/2011 MA TRẬN ĐÒ Nội dung Nhận biết Thông hiểu Vận dụng Tổng TNKQ TL TNKQ TL TNKQ TL Tính chất hóa học của oxit Biết tính chất hóa học của oxit Phân biệt được oxit với chất khác dựa vào tính chất hóa học (2) 0,5 điểm (1) 0,25 điểm (3) 0,75 đ Một số oxit quan trọng Biết nguyên liệu sản xuất SO2 và CaO, tính chất CaO (3) 0,5 điểm (3) 0,75 đ Tính chất hóa học của axit Biết tính chất hóa học của axit Trình bày lại tính chất hóa học của axit -Tính nồng độ mol của axit - Viết PTHH (2) 0,5 điểm (1) 0,25điểm (1) 0,25điểm (2) 1 điểm (6) 2,25 đ Một số axit quan trọng - Chỉ ra được tính chất hóa học của và quá trình sản xuất H2SO4 - Giới thiệu nhận biết muối sunfat - Trình bày lại tính chất hóa học của axit - Quá trình sản xuất H2SO4 - Phân biệt được axit với các muối -Tính toán liên quan đến PTHH ( thể tích chất khí, nồng độ mol) (3) 0,5 điểm (1) 0,25điểm (2) 3,5 điểm (3) 2,5 điểm (9) 6,25 đ Tổng cộng (10) 2,0 điểm (3) 0,75điểm (2) 3,5 điểm (1) 0,25 đ (5) 3,5 điểm (21) 10 đ Ư A : §Ò Bµi Câu 1 (3đ) Ghi l¹i ®¸p ¸n ®óng trong c¸c c©u sau. 1. Dãy oxit nào sau đây vừa tác dụng với nước, vừa tác dụng với dung dịch bazơ a. CaO, CuO b. CO, Na2O c. CO2, SO2 d. P2O5, MgO 2. Lưu huỳnh đioxit được tạo thành từ cặp chất nào sau đây? a. Na2SO3 và H2O b. Na2SO3 và NaOH c. Na2SO4 và HCl d. Na2SO3 và H2SO4 3. Chất nào sau đây được dùng để sản xuất vôi sống a. CaCO3 b. NaCl c. K2CO3 d. Na2SO4 4. Phản ứng giữa dung dịch HCl và NaOH là phản ứng a. Hóa hợp b. Trung hòa c. Thế d. Phân hủy 5. Trong công nghiệp, sản xuất axit sunfuric qua mấy công đoạn a. 1 b. 2 c. 3 d. 4 6.Oxit vừa tan trong nước vừa hút ẩm là: a. SO2 b. CaO c. Fe2O3 d. Al2O3 7. Cặp chất nào sau đây tác dụng với nhau sinh ra chất khí cháy trong không khí với ngọn lửa màu xanh? a. Zn + HCl b. ZnO + HCl c. Zn(OH)2+ HCl d. NaOH + HCl 8. Cặp chất nào sau đây xảy ra phản ứng: a. Na2O + NaOH b. Cu + HCl c. P2O5 + H2SO4 loãng d. Cu + H2SO4 đặc, nóng 9. Để loại bỏ khí CO2 có lẫn trong hỗn hợp O2 và CO2 . Người ta cho hỗn hợp đi qua dung dung dịch chứa a. HCl b. Na2SO4 c. NaCl d. Ca(OH)2 10. Oxit nào sau đây tác dụng với nước tạo thành dung dịch bazơ a. SO2 b. Na2O c. CO d. Al2O3 11. Axit sunfuric loãng tác dụng được với dãy chất nào sau đây a. Zn, CO2, NaOH b. Zn, Cu, CaO c. Zn, H2O, SO3 d. Zn, NaOH, Na2O 12. Trung hòa 100ml dung dịch HCl cần vừa đủ 50ml dung dịch NaOH 2M. Hãy xác định nồng độ mol dung dịch HCl đã dùng: a. 2M b. 1M c. 0,1M d. 0,2M Câu 2(1,5đ) Viết phương trình hóa học cho mỗi chuyển đổi hóa học sau và ghi rõ điều kiện phản ứng (nếu có) FeS2 SO2 SO3 H2SO4 Câu 3(1,5đ) Bằng phương pháp hóa học hãy phân biệt các dung dịch mất nhãn sau: Na2SO4, HNO3, HCl, NaCl đựng riêng biệt trong các lọ không dán nhãn. Viết PTHH minh họa. C©u 4(4®) Hoµ tan hoµn toµn 9,3 gam Na2O vµo níc thu ®îc 300 gam dung dÞch A cã D =1,2(g/ml) H·y tÝnh. a) TÝnh C% vµ CM cña dung dÞch A. b) Cho 5,6 lÝt khÝ CO2 vµo dung dÞch A sau khi ph¶n øng x¶y ra h·y tÝnh CM c¸c chÊt cã trong dung dÞch sau ph¶n øng. BiÕt thÓ tÝch dung dÞch kh«ng thay ®æi §¸p ¸n - BiÓu ®iÓm C©u ý §¸p ¸n §iÓm 1 3,0 Mỗi đáp án đúng được 0,25 đ Ý 1 2 3 4 5 6 7 8 9 10 11 12 Đ.A c d a b c b a d d b d b 2 1,5 4FeS2 + 1102 2Fe2O3 + 8SO2 2SO2 + O2 2SO3 SO3 + H2O H2SO 4 0,5 0,5 0,5 3 1,5 Dùng quỳ tím nhận được dung dịch HCl, HNO3 làm quỳ tím chuyển màu đỏ (nhóm A), NaCl và Na2SO4 không làm đổi màu quỳ tím (nhóm B). Dùng dung dịch AgNO3 nhận ra HCl tạo kết tủa trắng HNO3 không tạo kết tủa Dùng BaCl nhận ra Na2SO4 tạo kết tủa và NaCl không có hiện tượng gì. AgNO3 + HCl AgCl + HNO3 BaCl2 + Na2SO4 BaSO4 + 2NaCl 0,5 0,5 0,5 4 4,0 a 2,0 nNaO = 9,3 : 62 = 0,15(mol) PTHH: Na2O + H2O ® 2NaOH 1mol 2mol 0,15mol 0,3mol mNaOH = 0,3 x 40 = 12(g) C%NaOH = (12 : 300) x 100 = 4(%). Vdd = 300 : 1,2 = 250(ml) = 0,25(lÝt). CMNaOH = 0,3 : 0,25 = 1,2(M). 0,25 0,25 0,25 0,25 0,5 0,25 0,25 b 2,0 nCO = 5,6 : 22,4 = 0,25(mol). TØ lÖ: nNaOH : nCO = 0,3 : 0,25. vËy s¶n phÈm t¹o 2 muèi. Gäi sè mol NaHCO3 lµ x mol vµ sè mol cña Na2CO3 lµ y mol. (x,y > 0). PTHH: NaOH + CO2 ® NaHCO3 (1) xmol xmol xmol 2NaOH + CO2 ® Na2CO3 + H2O (2) 2ymol ymol ymol Tõ (1) vµ (2) ta cã hÖ ph¬ng tr×nh. x + 2y = 0,3 (a) x = 0,2 x + y = 0,25 (b) y = 0,05 CMNaHCO = 0,2 : 0,25 = 0,8(M). CMNaCO = 0,05 : 0,25 = 0,2(M). 0,25 0,25 0,25 0,25 0,25 0,25 0,25 0,25
Tài liệu đính kèm:
 TUẦN 5 TIẾT 10.doc
TUẦN 5 TIẾT 10.doc





