Giáo án Tuần 13 - Tiết 25 - Kiểm tra 45 phút môn hóa học
Bạn đang xem tài liệu "Giáo án Tuần 13 - Tiết 25 - Kiểm tra 45 phút môn hóa học", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
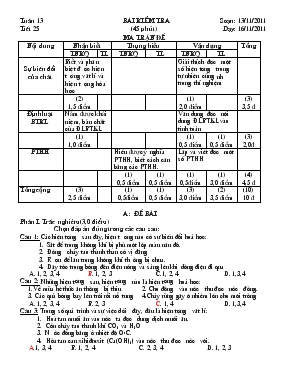
Tuần 13 bài kiểm tra Soạn: 13/11/2011 Tiết 25 (45 phút) Dạy: 16/11/2011 MA TRẬN Đề Nội dung Nhận biết Thụng hiểu Vận dụng Tổng TNKQ TL TNKQ TL TNKQ TL Sự biến đổi của chất Biết và phân biệt được hiện tượng vật lí và hiện tượng hóa học Giải thích được một số hiện tượng trong tự nhiên cũng như trong thí nghiệm (2) 1,5 điểm (1) 2,0 điểm (3) 3,5 đ Định luật BTKL Nắm được khái niệm, bản chất của ĐLBTKL Vận dụng được nội dung ĐLBTKL vào tinh toán (1) 1,0 điểm (1) 0,5 điểm (1) 0,5 điểm (3) 2,0đ PTHH Hiểu được ý nghĩa PTHH, biết cách cân bằng các PTHH. Lập và viết được một số PTHH (1) 0,5 điểm (1) 0,5 điểm (1) 0,5điểm (1) 3,0 điểm (4) 4,5 đ Tổng cộng (3) 2,5 điểm (1) 0,5điểm (1) 0,5 điểm (3) 3,0 điểm (2) 3,5 điểm (10) 10 đ A : Đề Bài Phần I. Trắc nghiêm (3,0 điểm) Chọn đáp án đúng trong các câu sau: Câu 1: Các hiện t ượng sau đây, hiện tư ợng nào có sự biến đổi hoá học: Sắt để trong không khí bị phủ một lớp màu nâu đỏ. Đường cháy tạo thành than có vị đắng Rư ợu để lâu trong không khí thư ờng bị chua. Dây tóc trong bóng đèn điện nóng và sáng lên khi dòng điện đi qua A. 1, 2, 3, 4 B. 1, 2, 3 C.1, 2, 4 D. 1,3,4 Câu 2: Những hiện t ượng sau, hiện t ượng nào là hiện t ượng hoá học: 1.Về mùa hè thức ăn th ường bị thiu 2. Cho đường vào nước thu được nước đường. 3. Các quả bóng bay lên trời rồi nổ tung 4.Cháy rừng gây ô nhiễm lớn cho môi trường A. 1, 2, 3, 4 B. 2, 3 C. 1, 4 D. 1,3,4 Câu 3: Trong số quá trình và sự việc d ưới đây, đâu là hiện t ượng vật lí: Hoà tan muối ăn vào nước ta đ ược dung dịch muối ăn. Cồn cháy tạo thành khí CO2 và H2O Nư ớc đóng băng ở nhiệt độ OoC. Hòa tan can xihiđroxit (Ca(OH)2) vào nước thu được nước vôi. A.1, 3, 4 B. 1, 2, 4 C. 2, 3, 4 D. 1, 2, 3 Câu 4: Cho phương trình hóa học: aAl2O3 + bHCl cAlCl3 + dH2O. Các hệ số a,b,c và d nhận các giá trị lần lượt là: A: 2,6,2,3. B: 1,6,2,3. C: 1,6,3,2. D: 2,6,3,2. Câu 5: Cho sơ đồ phản ứng: Al(OH)y + H2SO4 -> Alx(SO4)y + H2O Với x y thì giá trị thích hợp của x, y lần l ợt là: A. 1 và 2 B. 2 và 3 C. 2 và 4 D. 3 và 4 Câu 6: Đốt cháy 6,2 kg P cần 8kg khí O2. Khối l ượng P2O5 tạo ra là: A. 1,8kg B. 18 kg C. 14,2 kg D. 4,2kg Câu 7: Đốt cháy 6kg S thu đ ược là 12kg khí SO2. Khối l ượng O2 đã phản ứng là: A. 18,0kg B. 6,0kg C. 12 kg D.1,8kg Câu 8: Cho 5,4g Al tác dụng với dung dịch H2SO4 tạo ra 34,2g Al2(SO4)3 và 0,6 g khí H2. Khối lư ợng H2SO4 đã dùng là: A. 28,8g B. 28,2g C. 39,0g D. 29,4g Câu 9: Cho K vào nước xảy ra phản ứng: K + H2O -- KOH + H2. Các hệ số thích hợp trong phản ứng đó lần lượt là: A: 1,1,1,1. B: 2,2,2,1. C: 1,2,1,1. D: 1,2,1,2. Câu 10: Cho PTHH: xZn + yHCl zZnCl2 + tH2. Các hệ số x,y,z,t lần lượt là: A: 1,2,1,1. B: 2,1,1,1. C: 1,2,2,1. D: 1,2,1,2. Câu 11: Cho 9 gam C tác dụng với Fe2O3 nung ở nhiệt độ cao, kết thúc phản ứng thu được 56 gam Fe và 33 gam CO2. Khối lượng Fe2O3 là: A: 98g. B: 32g. C: 80g. D: 88g. Câu 12: Đốt cháy hoàn toàn 3,1 gam P trong bình chứa 4,8 gam O2 sau phản ứng thu được 7,1 gam P2O5. Khối lượng oxi dư là: A: 0,8 gam. B: 4,0 gam. C: 5,4 gam. D: 4,8 gam. Phần II. Tự luận (7,0 điểm) Câu 1(3điểm): Cho 5,4 gam Al tác dụng với dung dịch H2SO4 sau phản ứng thu được 17,1 gam Al2(SO4)3 và 1,2 gam H2. Viết phương trình hóa học của phản ứng trên. Cho biết tỉ lệ các chất trong phản ứng. Tính khối lượng H2SO4 phản ứng. Câu 2(4điểm): Hoàn thành các phương trình hóa học sau: 1. FeS2 + O2 Fe2O3 + SO2. 5. Al2O3 Al + 2. Al + H2SO4 Al2(SO4)3+ H2O + SO2 6. P + P2O5 3. Fe(OH)3 Fe2O3 + H2O 7. Al + Fe3O4 Al2O3 + Fe 4. Fe3O4 + H2SO4 Fe2(SO4)3 + H2O + SO2 8. Fe + FeCl3 B: đáp án - biểu điểm Câu ý Đáp án Điểm Phần I trắc nghiêm: Mỗi câu trả lời đúng được 0,25 điểm Câu 1 2 3 4 5 6 7 8 9 10 11 12 Đ. án B C A B B C B D B A C A 3,0 Phần II – tự luận 7,0 1 3,0 1 1,5 2Al + 3H2SO4 Al2(SO4)3 + 3H2 Tỉ lệ các chất trong phương trình: Al : H2SO4 : Al2(SO4)2: H2O = 2 : 3 : 1 : 3 1,0 0,5 2 1,5 áp dụng ĐLBTKL: mAl + mH = mAl + mH 5,4 + mH = 17,1 + 1,2 mH = 17,1 + 1,2 – 5,4 mH = 12,9 (g) 0,5 0,5 0,5 2 4,0 1. 4FeS2 + 11O2 2Fe2O3 + 8SO2. 2. 2Al + 6H2SO4 Al2(SO4)3+ 6H2O + 3SO2 3. 2Fe(OH)3 Fe2O3 + 3H2O 4. 2Fe3O4 + 10H2SO4 3Fe2(SO4)3 + 10H2O + SO2 5. 2Al2O3 4Al + 3O2 6. 4P + 5O2 2P2O5 7. 8Al + 3Fe3O4 4Al2O3 + 9Fe 8. 2Fe + 3Cl2 2FeCl3 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5
Tài liệu đính kèm:
 TUAN 12 - TIET 25.doc
TUAN 12 - TIET 25.doc





