Đề kiểm tra thi học kì I, năm học 2015 - 2016 môn: Hóa học 8 thời gian 45 phút
Bạn đang xem tài liệu "Đề kiểm tra thi học kì I, năm học 2015 - 2016 môn: Hóa học 8 thời gian 45 phút", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
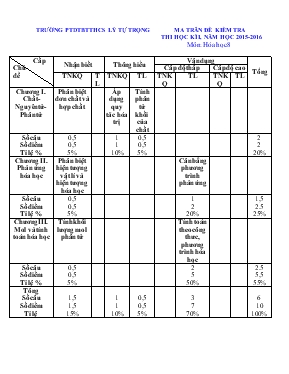
TRƯỜNG PTDTBTTHCS LÝ TỰ TRỌNG MA TRÂN ĐỀ KIỂM TRA THI HỌC KÌ I, NĂM HỌC 2015-2016 Môn: Hóa học 8 Cấp độ Chủ đề Nhận biết Thông hiểu Vận dụng Tổng Cấp độ thấp Cấp độ cao TNKQ TL TNKQ TL TNKQ TL TNKQ TL Chương I. Chất- Nguyên tử- Phân tử Phân biệt đơn chất và hợp chất Áp dụng quy tăc hóa trị Tính phân tử khối của chất Số câu Số điểm Tỉ lệ % 0,5 0,5 5% 1 1 10% 0,5 0,5 5% 2 2 20% Chương II. Phản ứng hóa học Phân biệt hiện tượng vật lí và hiện tượng hóa học Cân bằng phương trình phản ứng Số câu Số điểm Tỉ lệ % 0,5 0,5 5% 1 2 20% 1,5 2.5 25% Chương III. Mol và tính toán hóa học Tính khối lượng mol phân tử Tính toán theo công thưc, phương trình hóa học Số câu Số điểm Tỉ lệ % 0,5 0,5 5% 2 5 50% 2.5 5,5 55% Tông Số câu Số điểm Tỉ lệ 1,5 1,5 15% 1 1 10% 0,5 0,5 5% 3 7 70% 6 10 100% TRƯỜNG PTDTBTTHCS LÝ TỰ TRỌNG ĐỀ KIỂM TRA THI HỌC KÌ I, NĂM HỌC 2015-2016 Môn: Hóa học 8 Thời gian 45 phút Điểm Họ và Tên..Số báo danh.... Lớp Trường . Đề bài I. Trắc nghiệm : (3 điểm) Khoanh tròn vào đáp án đúng Câu1: ( 1 điểm ) mỗi đáp án đúng 0,5 điểm 1. Dãy công thức hóa học sau đây toàn là hợp chất : a. H2O, O3, CO2, Na2O b. CuCl2 , Al2O3, MgO , O2 c. K2O , ZnO, H2O, CuO d. BaO , Mn , CO , SO3 2. Khối lượng mol phân tử nitơ bằng : a. 14 b. 26 c. 16g d. 28g Câu 2: ( 1 điểm ) mỗi ý đúng 0,5 điểm 1. Nguyên tố R hợp với oxi có CTHH là R2O3.Trong CTHH nào sau đây R có hóa trị bằng hóa trị của R trong hợp chất trên : a. RCl3 b. RCl2 c. RCl d. RCl4 2. Hiện tượng sau đây là hiện tượng hóa học: a. Khi nung nóng nến chảy lỏng rồi thành hơi b. Khi nung nóng ở nhiệt độ cao thủy tinh nóng đỏ dễ dàng uốn cong được c. Cháy rừng gây ô nhiễm môi trường d. Quả bóng chứa khí bị nổ tung khi bay trên cao Câu 3: (1 điểm ) mỗi đáp án đúng 0,5 điểm 1. Cho biết công thức hoá học của hợp chất của nguyên tố X với O và hợp chất của nguyên tố Y với H như sau: X2O3 và YH2 . Hãy chọn công thức nào là đúng cho hợp chất X và Y(vd) A. X2Y3 B. X3Y C. XY3 D. X3Y2 2. Phân tử khối của hợp chất KMnO4 là A. 98 ; B.158 ; C. 160 ; D. 80 II. Tự luận : (7 điểm) Câu 1. Cho sơ đồ phản ứng sau : (2điểm) a. K + H2O à KOH + H2 b. Na + O2 à Na2O Hãy cân bằng PTHH . C©u 2. TÝnh thµnh phÇn phÇn tr¨m cña c¸c nguyªn tè trong c«ng trøc ho¸ häc sau: a. CuSO4 b. Ba3(PO4)2 (2 điểm) C©u 3. §èt 5,4 gam nh«m (Al) trong khÝ oxy (O2) t¹o thµnh muèi nh«m oxit (Al2O3) a. LËp ph¬ng tr×nh ph¶n øng ho¸ häc . b. TÝnh thÓ tÝch khÝ oxy (®ktc) cÇn dïng ®Ó ®èt ch¸y lîng nh«m trªn . c. TÝnh khèi lîng cña muèi nh«m oxit t¹o thµnh sau ph¶n øng. Cho biªt : Al = 27 ; O = 16 (3 điểm) Hết Đáp án Điểm I. Trắc nghiệm Câu 1. 1-c, 2-d; Câu 2. 1-a , 2-c; Câu 3. 1-a, 2-a 3 II. Tự luận: (7 điểm ) Câu 1 a. 2K + 2 H2O à 2KOH + H2 b. 4Na + O2 à 2Na2O C©u 2. a. CuSO4 = 64 + 32 + 64 = 160 gam 64 x 100% % Cu = = 40 % 160 32 x 100% % S = = 20 % 160 % O = 100 - 40 - 20 = 40 % b. Ba3(PO4)2 = 411 + 62 + 128 = 601 gam 411 x 100% %Ba = = 68,4 % 601 62 x 100 % %P = = 10,3% 601 %O = 100 - 68,4 - 10,3 = 24,9% C©u 3. a. ph¬ng tr×nh ph¶n øng: 4Al + 3O2 2Al2O3 5,4 b. Theo bµi ra ta cã sè mol Al = = 0,2 mol 27 theo ph¬ng tr×nh : 4Al + 3O2 2Al2O3 4mol 3mol 2mol 0,2mol x mol y mol 0,2 x 3 Sè mol cña O2 = x = = 0,15 mol 4 vËy thÓ tÝch khi oxi cÇn dïng lµ: 22,4 x 0,15 = 3,36 lÝt 0,2 x 2 c. Sè mol cña muèi Al2O3 = y = = 0,1 mol 4 VËy khèi lîng muèi t¹o thµnh lµ: 0,1 x 102 = 10,2 gam 1 1 1 1 1 1 1
Tài liệu đính kèm:
 de_kiem_tra_hoc_ki_I_Hoa_8.doc
de_kiem_tra_hoc_ki_I_Hoa_8.doc





