Đề kiểm tra học kỳ I, môn Hóa 8 năm học 2014-2015 Trường Thcs Đại Minh
Bạn đang xem tài liệu "Đề kiểm tra học kỳ I, môn Hóa 8 năm học 2014-2015 Trường Thcs Đại Minh", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
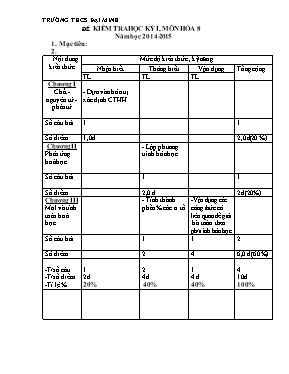
TRƯỜNG THCS ĐẠI MINH §Ò KIỂM TRA HỌC KỲ I, MÔN HÓA 8 Năm học 2014-2015 Mục tiêu: Nội dung kiến thức Mức độ kiến thức , kỹ năng Nhận biết Thông hiểu Vận dụng Tổng cộng TL TL TL Chương I Chất - nguyên tử - phân tử - Dựa vào hóa trị xác định CTHH Số câu hỏi 1 1 Số điểm 1,0đ 2,0đ(20 %) Chương II Phản ứng hoá học - Lập phương trình hóa học. Số câu hỏi 1 1 Số điểm 2,0 đ 2đ(20% ) Chương III Mol và tính toán hoá học - Tính thành phần % các n.tố. -Vận dụng các công thức có liên quan để giải bài toán theo ph/trình hóa học. Số câu hỏi 1 1 2 Số điểm 2 4 6,0 đ (60%) -T/số câu -T/số điểm -Tỉ lệ % 1 2đ 20% 2 4đ 40% 1 4 đ 40% 4 10đ 100% 100% ĐỀ KIỂM TRA HỌC KỲ I (NĂM HỌC 2014-2015) MÔN HOÁ 8 Câu 1. (2 đ) Lập công thức hóa học của những hợp chất tạo bởi: Na và SO4 , Mg và O , Al và CO3 , Al và NO3 Câu 2. (2,0 đ) Tính thành phần % về khối lượng của Fe có trong hợp chất sau:Fe2O3 Câu 3: (2 đ) Chọn hệ số viết thành PTHH với các sơ đồ phản ứng cho dưới đây : a. Fe + O2 t0 Fe3O4 b. SO2 + O2 t0 SO3 c. Fe(OH)3 t0 Fe2O3 + H2O d. Fe3O4 + HCl FeCl2 + FeCl3 + H2O Câu 4 : (4đ) Cho 13 gam Zn tác dụng với một lượng dung dịch axitclohidric (HCl) vừa đủ người ta thu được muối kẽm clorrua (ZnCl2) và khí hidro. Viết phương trình phản ứng hóa học xảy ra ? Tính khối lượng HCl cần dùng ? Tính khối lượng muối ZnCl2 thu được ? Tính thể tích H2 sinh ra ở điều kiện tiêu chuẩn ? ( Cho biết : Zn = 65 ; H = 1 ; Cl = 35,5 ; Fe = 56 ; S = 32 ; O = 16 ) ĐÁP ÁN - BIỂU ĐIỂM ĐỀ KIỂM TRA HỌC KÌ I MÔN : HOÁ 8 NĂM HỌC 2013-2014 Câu 1: (2 đ iểm) Lập mỗi công thức đúng cho 0,5 đ Câu 2: (2 đ iểm) Fe2O3 MFe2O3 = 112 + 48 = 160g (0,5đ) % Fe = 112 : 160 . 100% = 70% (0,5đ) Câu 3: (2 đ iểm) a. 3Fe + 2O2 t0 Fe3O4 (0,5đ) b. 2SO2 + O2 t0 2SO3 (0,5đ) c. 2 Fe(OH)3 t0 Fe2O3 + 3 H2O (0,5đ) d. Fe3O4 + 8HCl FeCl2 + 2FeCl3 + 4H2O (0,5đ) Câu 4:(4 đ iểm) nZn = 13 : 65 = 0,2 (mol) (0,5đ) a. Zn + 2HCl ZnCl2 + H2 (0,5đ) 1mol 2mol 1mol 1mol 0,2mol x mol y mol z mol b. x = nHCl = 0,4mol => mHCl = 0,4 x 36,5 = 14,6 (gam) (0,5đ) c. y = nZnCl2 = 0,2mol => mZnCl2 = 0,2 x 136 = 27,2 (gam) (0,5đ) d. z = nH2 = 0,2mol => VH2 = 0,2 x 22,4 = 4,48 (lit ) (0,5đ) CM duyệt: Người ra đề Hồ Thị Tùng
Tài liệu đính kèm:
 Hóa 8.doc
Hóa 8.doc





