Đề kiểm tra học kỳ 1 môn : Hoá học lớp : 9
Bạn đang xem tài liệu "Đề kiểm tra học kỳ 1 môn : Hoá học lớp : 9", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
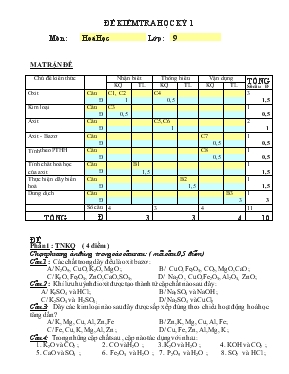
ĐỀ KIỂM TRA HỌC KỲ 1 Môn : Hoá Học Lớp : 9 MA TRẬN ĐỀ Chủ đề kiến thức Nhận biết Thông hiểu Vận dụng TỔNG Số câu Đ KQ TL KQ TL KQ TL Oxit Câu C1, C2 C4 3 Đ 1 0,5 1,5 Kim loại Câu C3 1 Đ 0,5 0,5 Axit Câu C5,C6 2 Đ 1 1 Axit - Bazơ Câu C7 1 Đ 0,5 0,5 Tính theo PTHH Câu C8 1 Đ 0,5 0,5 Tính chất hoá học của axit Câu B1 1 Đ 1,5 1,5 Thực hiện dãy biến hoá Câu B2 1 Đ 1,5 1,5 Dung dịch Câu B3 1 Đ 3 3 Số câu 4 3 4 11 TỔNG Đ 3 3 4 10 ĐỀ Phần 1 : TNKQ ( 4 điểm ) Chọn phương án đúng trong các câu sau : ( mỗi câu 0,5 điểm ) Câu 1 : Các chất trong dãy đều là oxit bazơ : A/ N2O5, CuO, K2O, MgO ; B/ CuO, Fe2O3, CO2, MgO,CaO ; C/ K2O, Fe2O3, ZnO, CaO, SO3, D/ Na2O , CuO, Fe2O3, Al2O3, ZnO ; Câu 2 : Khí lưu huỳnh đioxit được tạo thành từ cặp chất nào sau đây : A/ K2SO4 và HCl ; B/ Na2SO3 và NaOH ; C/ K2SO3 và H2SO4 ; D/ Na2SO4 và CuCl2 Câu 3: Dãy các kim loại nào sau đây được sắp xếp đúng theo chiều hoạt động hoá học tăng dần ? A/ K, Mg, Cu, Al, Zn, Fe B/ Zn, K, Mg, Cu, Al, Fe; C/ Fe, Cu, K, Mg, Al, Zn ; D/ Cu, Fe, Zn, Al, Mg, K ; Câu 4: Trong những cặp chất sau , cặp nào tác dụng với nhau : 1. K2O và CO2 ; 2. CO và H2O ; 3. K2O và H2O ; 4. KOH và CO2 ; 5. CaO và SO3 ; 6. Fe2O3 và H2O ; 7. P2O5 và H2O ; 8. SO2 và HCl ; A/ 1,2,3,4,6,7 B/ 1,3,4,5,7 C/ 2,3,4,5,6 D/ 1,2,3,4,5,6 Câu 5 : H2 SO4 loãng không phản ứng với các chất trong các tập hợp sau : A. Fe, Al, Zn. B. CuO, Al2O3, CaCO3. C.Cu, Ag, Hg, NaCl, D. Cu (OH)2, Fe (OH)3. Câu 6 : Sau khi đốt phôtpho đỏ trong bình có một it nước. Lắc bình một lúc, trong bình có một dung dịch.. DD trong bình làm quì tím chuyển màu thành : A/ Xanh , B/ Đỏ , C/ Mất màu , D/ Vẫn màu tím . Câu 7 :. Nhận biết các dung dịch : HCl , NaOH và H2SO4 ta có thể dùng các cách sau : A/ Chỉ dùng thêm quì tím. B/ Chỉ dùng thêm dung dịch BaCl2 . C/ Dùng quì tím và dung dịch BaCl2 . D/ Tất cả đều đúng . Câu 8 : Phân tử khối của hợp chất M là 160 và thành phần % về khối lượng của các nguyên tố trong hợp chất : sắt (70%) và oxi (30%). Công thức phân tử hợp chất M là : A/ FeO B/ Fe2O3 C/ Fe3O4 D. Fe2O Phần 2 : TỰ LUẬN ( 6 điểm ) Câu 1 : Trình bày tính chất hoá học của axit clohidric . Viết PTHH minh hoạ. Câu 2 : Viết PTHH thực hiện những chuyển đổi hoá học sau : SO2 à H2SO3 à Na2SO3 à SO2 Câu 3 : Cho 15,5 g Na2O tác dụng với nước được 0,5 lít dung dịch A. Tính nồng độ M của dung dịch A . Tính thể tích dung dịch H2SO4 20 % ( d = 1,14g/ml ) cần để trung hoà dung dịch A . Tính nồng độ M của chất có trong dung dịch sau phản ứng . ĐÁP ÁN – HƯỚNG DẪN CHẤM Phần 1 : ( 4 điểm ) Câu 1 2 3 4 5 6 7 8 Ph.án đúng A C D B C B C B Phần 2 : ( 6 điểm ) Câu 1: Trình bày và viết PTHH minh hoạ đúng, đủ (1,5đ ) Câu 2 : Viết đúng 3 PTHH (1,5đ ) Câu 3 :a) Tính đúng CM của dung dịch A : 1mol/l (1đ) b) Tính đúng V dd H2SO4 20 % = 107,5 ml . (1đ) c) Tính đúng CM của dd Na2SO4 = 0,41 M. (1đ )
Tài liệu đính kèm:
 De_thi_Hoa_HKI.doc
De_thi_Hoa_HKI.doc





