Đề kiểm tra học kì II (2010 - 2011) hóa học 9 thời gian: 45 phút trường THCS thị trấn Kiên Lương 1
Bạn đang xem tài liệu "Đề kiểm tra học kì II (2010 - 2011) hóa học 9 thời gian: 45 phút trường THCS thị trấn Kiên Lương 1", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
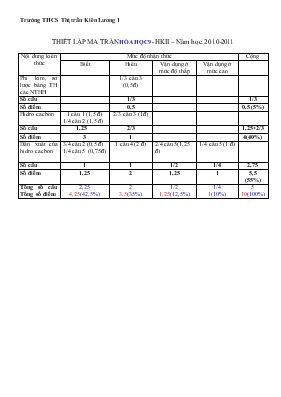
Trường THCS Thị trấn Kiên Lương 1 THIẾT LẬP MA TRẬN HÓA HỌC 9 - HKII – Năm học: 2010-2011 Nội dung kiến thức Mức độ nhận thức Cộng Biết Hiểu Vận dụng ở mức độ thấp Vận dụng ở mức cao Phi kim, sơ lược bảng TH các NTHH 1/3 câu 3 (0,5đ) Số câu 1/3 1/3 Số điểm 0,5 0,5 (5%) Hidro cacbon 1 câu 1 (1,5 đ) 1/4 câu 2 (1,5 đ) 2/3 câu 3 (1đ) Số câu 1,25 2/3 1,25+2/3 Số điểm 3 1 4(40%) Dẫn xuất của hidro cacbon 3/4 câu 2 (0,5 đ) 1/4 câu 5 (0,75đ) 1 câu 4 (2 đ) 2/4 câu 5(1,25 đ) 1/4 câu 5 (1 đ) Số câu 1 1 1/2 1/4 2,75 Số điểm 1,25 2 1,25 1 5,5 (55%) Tổng số câu Tổng số điểm 2,25 4,25(42,5%) 2 3,5(35%) 1/2 1,25(12,5%) 1/4 1(10%) 5 10(100%) Phòng GD&ĐT huyện Kiên Lương Trường THCS Thị trấn Kiên Lương 1 ĐỀ KIỂM TRA HỌC KÌ II (2010-2011) HÓA HỌC 9 Thời gian: 45 phút Đề chẵn Câu 1 (1,5điểm) Trình bày tính chất hóa học của etylen. Viết phương trình minh họa Câu 2 (2điểm) Viết công thức phân tử của các chất có tên sau: tinh bột, saccarozơ, rượu etylic, axetilen Câu 3 (1,5điểm) Bằng phương pháp hóa học nhận biết ba lọ khí mất nhãn đựng trong ba lọ riêng biệt sau: Cl2, CH4, C2H2. Viết phương trình, nếu có. Câu 4 (2điểm) Thực hiện chuyển đổi sau, ghi điều kiện, nếu có. Tinh bột → (1) Glucozơ →(2) Rượu etylic →(3) Axit axetic →(4) Axetat canxi. Câu 5 (3điểm) Hòa tan 4,8 gam magiê vào dung dịch axitaxetic 0,2M. a) Viết phương trình phản ứng. b) Tính thể tích hidro (ĐKTC). c) Tính thể tích dung dịch axit axetic cần dùng cho phản ứng. d) Giả sử cho toàn bộ lượng axit axetic trên tác dụng với kim loại R hóa trị I. Sau phản ứng thu được 32,8 gam muối. Xác định kim loại R. HẾT Phòng GD&ĐT huyện Kiên Lương Trường THCS Thị trấn Kiên Lương 1 ĐỀ KIỂM TRA HỌC KÌ II (2010-2011) HÓA HỌC 9 Thời gian: 45 phút Đề lẻ Câu 1 (1,5điểm) Trình bày tính chất hóa học của benzen. Viết phương trình minh họa Câu 2 (2điểm) Viết công thức phân tử của các chất có tên sau: xenlulozơ, glucozơ, metan, axit axetic. Câu 3 (1,5điểm) Bằng phương pháp hóa học nhận biết ba lọ khí mất nhãn đựng trong ba lọ riêng biệt sau: Cl2, CH4, C2H4. Viết phương trình, nếu có. Câu 4 (2điểm) Thực hiện chuyển đổi sau, ghi điều kiện, nếu có. Saccarozơ → (1) Glucozơ → (2) Rượu etylic → (3) Axit axetic → (4) Axetat bari. Câu 5 (3điểm) Hòa tan 9,6 gam magiê vào dung dịch axitaxetic 0,5M. a) Viết phương trình phản ứng. b) Tính thể tích hidro (ĐKTC). c) Tính thể tích dung dịch axit axetic cần dùng cho phản ứng. d) Giả sử cho toàn bộ lượng axit axetic trên tác dụng với kim loại R hóa trị I. Sau phản ứng thu được 78,4 gam muối. Xác định kim loại R. HẾT Trường THCS Thị trấn Kiên Lương 1 XÂY DỰNG ĐÁP ÁN VÀ THANG ĐIỂM HÓA HỌC 9 – HKII- 2010-2011 Đề chẵn Câu 1. Mỗi tính chất, kèm PTHH(0,5 đ) - Tác dụng với oxi: C2H4 + 3O2 → t0 2CO2 + 3H2O - Phản ứng cộng với brom: C2H4 + Br2 → C2H4Br2 - Phản ứng trùng hợp: +CH2=CH2+ CH2=CH2+... xt, p, t0 - CH2-CH2- CH2-CH2- Câu 2. Mỗi công thức đúng: 0,5đ (-C6H10O5-)n, C12H22O11, C2H6O, C2H2. Câu 3. Dẫn lần lượt từng khí qua dung dịch brom. (0,25 đ) -Khí làm mất màu dung dịch brom→ C2H2 (0,25 đ) C2H2 + 2Br2 →C2H2Br4. (0,25 đ) - Còn lại Cl2 , CH4. Nhúng giấy quỳ tím ẩm vào hai lọ khí còn lại. (0,25 đ) - Khí làm mất màu quỳ tím → Cl2. (0,25 đ) -Còn lại CH4. (0,25 đ) Câu 4. Mỗi phương đúng, đủ: 0,5đ (1) (-C6H10O5-)n + nH2O axit, t0 n C6H12O6 (2) C6H12O6 men rượu,30-32°C 2C2H5OH + 2CO2 (3) C2H5OH + O2 men giấm CH3COOH + H2O (4) 2CH3COOH + CaO → (CH3COO) 2Ca + H2O. Câu 5. a) 2CH3COOH + Mg → (CH3COO) 2Mg + H2. (0,75đ) b) Số mol của Mg = ( 0,75 đ) c) (0,5 đ) d) 2CH3COOH + 2R → 2CH3COOR + H2. Theo PT: (1đ) HẾT Trường THCS Thị trấn Kiên Lương 1 XÂY DỰNG ĐÁP ÁN VÀ THANG ĐIỂM: HÓA HỌC 9- HKII-2010-2011 Đề lẻ Câu 1. Mỗi tính chất, kèm PTHH(0,5 đ) - Tác dụng với oxi: 2C6H6 + 15O2 → t0 12CO2 + 6H2O - Phản ứng thế với brom: C6H6 + Br2 →Fe, t0 C6H5Br + HBr - Phản ứng cộng với hidro: C6H6 + H2 Ni, t0 C6H12 Câu 2. Mỗi công thức đúng: 0,5đ (-C6H10O5-)n, C6H12O6, CH4 ,C2H4O2 Câu 3. Dẫn lần lượt từng khí qua dung dịch brom. (0,25 đ) -Khí làm mất màu dung dịch brom → C2H4 (0,25 đ) C2H4 + Br2 →C2H4Br2. (0,25 đ) - Còn lại Cl2 , CH4. Nhúng giấy quỳ tím ẩm vào hai lọ khí còn lại. (0,25 đ) - Khí làm mất màu quỳ tím → Cl2. (0,25 đ) -Còn lại CH4. (0,25 đ) Câu 4. Mỗi phương đúng, đủ: 0,5đ (1) C12H22O11 + H2O axit, t0 C6H12O6 + C6H12O6 (2) C6H12O6 men rượu,30-32°C 2C2H5OH + 2CO2 (3) C2H5OH + O2 men giấm CH3COOH + H2O (4) 2CH3COOH + BaO → (CH3COO) 2Ba + H2O. Câu 5. a) 2CH3COOH + Mg → (CH3COO) 2Mg + H2. (0,75đ) b) Số mol của Mg = ( 0,75 đ) c) ( 0,5 đ) d) 2CH3COOH + 2R → 2CH3COOR + H2. Theo PT: (1đ) HẾT
Tài liệu đính kèm:
 de_thi_hoa_9.doc
de_thi_hoa_9.doc





