Đề kiểm tra 1 tiết (tiết 25 ) hóa học 8
Bạn đang xem 20 trang mẫu của tài liệu "Đề kiểm tra 1 tiết (tiết 25 ) hóa học 8", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
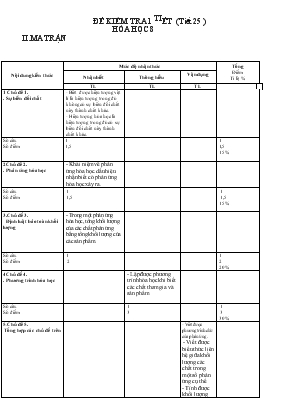
ĐỀ KIỂM TRA 1 TIẾT (Tiết 25 ) HÓA HỌC 8 II.MA TRẬN Nội dung kiến thức Mức độ nhận thức Tổng Điểm Tỉ lệ % Nhận biết Thông hiểu Vận dụng TL TL TL 1 Chủ đề 1. . Sự biến đổi chất - Biết được hiện tượng vật lí là hiện tượng trong đó không có sự biến đổi chất này thành chất khác. - Hiện tượng hóa học là hiện tượng trong đó có sự biến đổi chất này thành chất khác. Số câu Số điểm 1 1,5 1 1,5 15% 2Chủ đề 2. . Phản ứng hóa học - Khái niệm về phản ứng hóa học.dấu hiệu nhận biết có phản ứng hóa học xảy ra. Số câu Số điểm 1 1,5 1 1,5 15% 3.Chủ đề 3. Định luật bảo toàn khối lượng - Trong một phản ứng hóa học, tổng khối lượng của các chất phản ứng bằng tổng khối lượng của các sản phẩm. Số câu Số điểm 1 2 1 2 20% 4Chủ đề 4. . Phương trình hóa học - Lập được phương trình hóa học khi biết các chất tham gia và sản phẩm. Số câu Số điểm 1 3 1 3 30% 5.Chủ đề 5. Tổng hợp các chủ đề trên - Viết được phương trình chữ của phản ứng . - Viết được biểu thức liên hệ giữa khối lượng các chất trong một số phản ứng cụ thể. - Tính được khối lượng của một chất trong phản ứng khi biết khối lượng của các chất còn lại. Số câu Số điểm 1 2 1 2 20% TỔNG: Số câu Số điểm Tỉ lệ % 3 5 50% 1 3 30% 1 2 20% 5 10 đ 100% III.ĐỀ KIỂM TRA Câu 1:(1,5đ )Thế nào là hiện tượng vật lí ? cho ví dụ Câu 2: (1,5 đ )Phản ứng hóa học là gì? điều kiện để có phản ứng hóa học xảy ra? Câu 3: : (2 đ )Phát biểu định luật bảo toàn khối lượng? viết biểu thức theo định luật? Câu 4:(3 đ ) Lập phương trình hóa học của phản ứng sau: (3 đ ) a. Al + HCl - - -> AlCl3 + H2 . b. Fe2O3 + CO - - -> Fe + CO2 . c. P + O2 - - -> P2O5 Câu 5: (2 đ )Cho 65g kim loại Kẽm tác dụng với Axit Clohidric ( HCl) thu được 136g muối kẽm Clorua ( ZnCl2 ) và 2g khí hidro (H2 ). ( 2 đ ) a. Viết phương trình chữ của phản ứng . b. Viết biểu thức theo định luật . c. Tính khối lượng axit clohidric đã dùng. ....................HẾT.......................................... IV ĐÁP ÁN- THANG ĐIỂM Câu Noäi dung ñaùp aùn Bieåu ñieåm 1 Hiện tượng chất biến đổi mà không tạo ra chất mới được gọi là hiện tượng vật lí . Ví dụ :thủy tinh được thổi thành bình cầu . 1 ñieåm 0,5 ñieåm 2 Phản ứng hóa học là quá trình biến đổi từ chất này thành chất khác . Điều kiện : Các chất phải tiếp xúc với nhau . Có phản ứng cần đun nóng . Có phản ứng cần có thêm chất xúc tác. 1 ñieåm 0,5 ñieåm 3 3 Định luật :trong một phản ứng hóa học tổng khối lượng của sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng . Biểu thức : mA + mB à mC + mD 1 ñieåm 1 ñieåm 4 a. 2Al + 6 HCl à 2 AlCl3 + 3H2 . b. Fe2O3 +3 CO à 2 Fe + 3CO2 . c. 4P + 5 O2 à 2 P2O5 1 ñieåm 1 ñieåm 1 ñieåm 5 Kẽm + Axit Clohidric à kẽm Clorua + hidro Zn + 2HCl à ZnCl2 + H2 2. mZn + mHCl = mZnCl2 + mH2 3. mHCl = mZnCl2 + mH2 – mZn = 136 + 2 – 65 =73 g 0,5 ñieåm 0,5 ñieåm 0,5 ñieåm 0,5 ñieåm V. KẾT QUẢ : LỚP TSHS GIỎI KHAÙ TB YEÁU KEÙM SL TL SL TL SL TL SL TL SL TL 8A1 8A2 8A3 TC NHẬN XÉT ĐÁNH GIÁ : 1) Ưu điểm : 2) Tồn tại 3)Hướng khắc phục ------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------- Tröôøng THCS Suoái Ngoâ Họ và tên: . KIỂM TRA 1 TIEÁT Lớp: Môn: Hóa Học 8 TG: 45 Phuùt Điểm Lời Phê của giáo viên Câu 1:(1,5đ )Thế nào là hiện tượng vật lí ? cho ví dụ . .. .. Câu 2: (1,5 đ )Phản ứng hóa học là gì? điều kiện để có phản ứng hóa học xảy ra? . Câu 3: : (2 đ )Phát biểu định luật bảo toàn khối lượng? viết biểu thức theo định luật? .. Câu 4:(3 đ ) Lập phương trình hóa học vaø cho bieát tæ leä soá nguyeân töû, soá phaân töû cuûa caùc chaát trong moãi phaûn öùng sau: a. Mg+ HCl - - -> MgCl2 + H2 . b. Fe2O3 + CO - - -> Fe + CO2 . c. P + O2 - - -> P2O5 d. HgO - - -> Hg + O2 . . Câu 5: (2 đ )Cho 6,5(g) kim loại Kẽm tác dụng với Axit Clohidric ( HCl) thu được 13,6 (g) kẽm Clorua và 2(g) khí hidro (H2 ). a. Viết phương trình chữ của phản ứng . b. Viết biểu thức theo định luật . c. Tính khối lượng axit clohidric đã dùng. ........................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................... .................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................... Tröôøng THCS Suoái Ngoâ Họ và tên: . KIỂM TRA 1 TIEÁT Lớp: Môn: Hóa Học 8 TG: 45 Phuùt Điểm Lời Phê của giáo viên Câu 1:(1,5đ )Thế nào là hiện tượng hoùa hoïc ? cho ví dụ .. .. Câu 2: (1,5 đ )Phản ứng hóa học là gì? dấu hiệu để nhận biết có phản ứng hóa học xảy ra . .. .. Câu 3: : (2 đ )Phát biểu định luật bảo toàn khối lượng? viết biểu thức theo định luật? .. .. .. Câu 4 : ( 2 điểm ) Lập các phương trình hóa học vaø cho bieát tæ leä soá nguyeân töû, soá phaân töû cuûa caùc chaát trong moãi phaûn öùng sau: a. Al + Cl2 - - -> AlCl3 b. Fe (OH)3 - - -> Fe2O3 + H2O c. Na + O2 - - -> Na2O d. Fe + HCl ---> FeCl2 + H2 .. .. .. .. Câu 5: (3 đ )Cho 2,4 (g) kim loại Magie tác dụng với 7,2(g) Axit Clohidric ( HCl) thu được Magie Clorua và 2(g) khí hidro (H2 ). a. Laäp phương trình hoùa hoïc của phản ứng . b. Viết biểu thức theo định luật . c. Tính khối lượng Magie Clorua thu ñöôïïc. .. .. .. .. B. TÖÏ LUAÄN Caâu 5: ( 3 ñieåm) Cho sô ñoà caùc phaûn öùng hoaù hoïc sau: 1. Cu + Cl2 - - -> CuCl2 2. Fe2O3 + H2 - - -> Fe + H2O 3. Al + FeSO4 - - -> Al2(SO4)3 + Fe Laäp phöông trình hoaù hoïc vaø cho bieát tæ leä soá nguyeân töû, soá phaân töû cuûa caùc chaát trong moãi phaûn öùng a Caâu 6: (3 ñieåm) Cho 130g keõm (Zn) taùc duïng vöøa ñuû vôùi axit clohidric (HCl) ñöôïc 272g keõm clorua (ZnCl2 ) vaø 4g khí hidro (H2). Laäp phöông trình hoaù hoïc cuûa phaûn öùng . Vieát bieåu thöùc lieân heä veà khoái löôïng giöõa caùc chaát trong phaûn öùng. Tính khoái löôïng axit clohiric ñaõ tham gia phaûn öùng (3ñ) ÑAÙP AÙN A. TRAÉC NGHIEÄM Caâu 1: (1 ñieåm) 1. HTVL (0,25 ñ) 2. HTHH (0,25 ñ) 3. HTHH (0,25 ñ) 4.HTVL (0,25 ñ) Caâu 2: (1 ñieåm) phaûn öùng hoaù hoïc (0,25 ñ) lieân keát (0,25 ñ) soá löôïng (0,25 ñ) khoái löôïng (0,25 ñ) Caâu 3: ( 1 ñieåm) phöông aùn a: giaûm ñi (1ñ) Caâu 4: ( 1 ñieåm) Sai: b Ñuùng: a,c, d PHAÀN 2: TÖÏ LUAÄN Caâu 5: ( 3 ñieåm) 1. Cu + Cl2 à CuCl2 (0,75ñ) Tæ leä: soá nguyeân töû Cu : soá phaân töû Cl2 : soá phaân töû CuCl2 = 1 : 1 :1 (0,75ñ) 2.Fe2O3 + 3H2 à 2Fe + 3H2O (0,75ñ) 3. 2Al + 3FeSO4 à Al2(SO4)3 + 3Fe (0,75ñ) Caâu 6:( 3 ñieåm) 1. Zn + 2HCl à ZnCl2 + H2 (1ñ) 2. mZn + mHCl = mZnCl2 + mH2 (1ñ) 3. mHCl = mZnCl2 + mH2 – mZn = 272 + 4 – 130 = 146g (1ñ) ÑEÀ 2 PHAÀN 1: TRAÉC NGHIEÄM Caâu:1. (1ñieåm) Trong caùc hieän töôïng döôùi ñaây,haõy ghi hieän töôïng hoaù hoïc (HTHH) hoaëc hieän töôïng vaät lí (HTVL) vaøo choã coù caùc daáu chaám, sau moãi cuïm töø moâ taû hieän töôïng sao cho thích hôïp (1ñ) a) Röôïu loaõng ñeå laâu trong khoâng khí bò chua daàn. (.) b) Hoaø tan ñöôøng vaøo nöôùc thaønh nöôùc ñöôøng. (.) c) Daây saét ñeå ngoaøi khoâng khí bò phuû moät lôùp gæ maøu naâu ñoû. (.) d) Thanh ñoàng ñöôïc keùo thaønh caùc sôïi nhoû ñeå laøm daây ñieän. () Caâu 2: (1 ñieåm) Khoái löôïng ñoàng bò oxi hoaù do phaûn öùng vôùi khí oxi taïo thaønh ñoàng oxit. Vaäy khi nung noùng mieáng kim loaïi ñoàng trong khoâng khí ( coù khí oxi) thì khoái löôïng mieáng ñoàng seõ thay ñoåi nhö theá naøo? A. Giaûm ñi. B. Taêng leân. C. Khoâng thay ñoåi. Caâu 3: ( 1 ñieåm) Hoaøn thaønh caùc caâu sau ñaây baèng caùch theâm vaøo caùc cuïm töø thích hôïp: phaûn öùng hoaù hoïc, soá löôïng, khoái löôïng, lieân keát (1ñ) Trong dieãn ra söï thay ñoåi giöõa caùc nguyeân töû. Coøncaùc nguyeân töû khoâng thay ñoåi, vì vaäycaùc chaát ñöôïc baûo toaøn. Caâu 4: ( 1ñieåm) Trong caùc phaùt bieåu sau, phaùt bieåu naøo ñuùng, phaùt bieåu naøo sai. Em haõy vieát chöõ Ñ vaøo caâu phaùt bieåu ñuùng, chöõ S vaøo caâu phaùt bieåu sai: a) Khi caùc chaát coù phaûn öùng thì chính laø caùc phaân töû phaûn öùng vôùi nhau. b) Neán loûng chuyeån thaønh hôi laø hieän töôïng hoaù hoïc. c) Khoái löôïng cuûa caùc chaát saûn phaåm baèng khoái löôïng caùc chaát phaûn öùng. d) Trong phaûn öùng hoaù hoïc nguyeân töû khoâng bò phaân chia. PHAÀN 2: TÖÏ LUAÄN Caâu 5: ( 3 ñieåm) Cho sô ñoà caùc phaûn öùng hoaù hoïc sau: 1. Mg + Cl2 - - -> MgCl2 2. Al2O3 + H2 - - -> Al + H2O 3. Al + FeSO4 - - -> Al2(SO4)3 + Fe Laäp phöông trình hoaù hoïc vaø cho bieát tæ leä soá nguyeân töû, soá phaân töû cuûa caùc chaát trong moãi phaûn öùng a (3ñ) Caâu 6: ( 3 ñieåm) Canxi cacbonat (CaCO3) laø thaønh phaàn chính cuûa ñaù voâi. Khi nung ñaù voâi taïo thaønh voâi soáng (CaO) vaø khí cacbon ñioxit (CO2) thoaùt ra. a) Laäp PTHH cuûa phaûn öùng treân. b) Vieát coâng thöùc veà khoái löôïng caùc chaát trong phaûn öùng? c) Bieát raèng khi nung 5,6 taán ñaù voâi thì coù 2,2 taán khí cacbon ñioxit thoaùt ra. Tính khoái löôïng voâi soáng thu ñöôïc. Ñaùp aùn: Caâu 1: ( 1 ñieåm) a) HTHH b) HTVL c) HTHH d) HTVL Caâu 2: (1 ñieåm) b – taêng leân Caâu 3: (1 ñieåm) phaûn öùng hoaù hoïc (0,25 ñ) lieân keát (0,25 ñ) soá löôïng (0,25 ñ) khoái löôïng (0,25 ñ) Caâu 4: (1ñieåm) Sai: b Ñuùng: a,c, d PHAÀN 2: TÖÏ LUAÄN Caâu 5: (3ñieåm) 1. Mg + Cl2 MgCl2 soá nguyeân töû Mg: soá phaân töû Cl2: Soá phaân töû MgCl2 = 1 : 1 : 1 2. Al2O3 + 3 H2 2Al + 3 H2O 3. 2Al + 3 FeSO4 Al2(SO4)3 + 3 Fe Caâu 6: (3ñieåm) CaCO3 CaO + CO2 m CaCO = mCaO + mCO 5,6 taán = x taán + 2,2 taán Khoái löôïng voâi soáng thu ñöôïc: X =5,6 - 2,2 = 3,4 taán 4. Cuûng coá vaø luyeän taäp: thu baøi kieåm tra vaø nhaän xeùt tieát kieåm tra 5. Höôùng daãn hs hoïc ôû nhaø: Xem baøi 18: Mol – Tìm hieåu: Mol laø gì? Khoái löôïng mol laø gì? (oân laïi nguyeân töû khoái - baûng 1 tr42). Theå tích nol cuûa chaát khí. V. RUÙT KINH NGHIEÄM : ........................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................................ Hoï teân: ÑEÀ KIEÅM TRA 1 TIEÁT Lôùp: MOÂN : HOAÙ 8 I) Traéc nghieäm : Haõy choïn caâu traû lôùi ñuùng cho caùc caâu traû lôùi sau Caâu 1: Hieän töôïng naøo sau ñaây laø hieän töôïng vaâït lí ? A.Thuyû tinh noùng chaûy ñöôïc thoåi thaønh b ình caàu B. Röôïu ñeå laâu trong khoâng khí thöôøng bò chua C. Cho voâi soáng hoaø tan vaøo nöôùc ñöôïc voâi toâi D. Khi ñaùnh dieâm coù löûa baén ra Caâu 2: Hieän töôïng naøo sau laø hieän töôïng hoaù hoïc ? A. Möïc hoaø tan vaøo nöôùc B. Tröùng bò thoái C. Daây toùc boùng ñeøn ñieän noùng vaø saùng leân khi coù doøng dieän chaïy qua D. Söï keát tinh muoái aên Caâu 3: Phöông trình hoaù hoïc bieåu dieãn ngaén goïn A. Coâng thöùc hoaù hoïc B. Soá phaân töû cuûa caùc chaát trong phaûn öùng C. Phaûn öùng hoaù hoïc D. Chaát tham gia vaø saûn phaåm Caâu 4: Trong moät phaûn öùng hoaùhoïc chæ coù : A. Soá nguyeân töû thay ñoåi B. Soá phaân töû thay ñoåi C. Lieân keát caùc chaát thay ñoåi laøm cho phaûn öùng naøy bieán ñoåi thaønh phaûn öùng khaùc D. Lieân keát giöõa caùc nguyeân töû thay ñoåi laøm cho phaân töû naøy bieán ñoåi thaønh phaân töû khaùc Caâu 5. Cho sô ñoà phaûn öùng sau: Al(OH)y + H2SO4 - - -> Alx(SO4)y + H2O Haõy choïn x, y baèng caùc chæ soá thích hôïp naøo sau ñaây ñeå laäp ñöôïc phöông trình hoaù hoïc treân. A. x = 2, y = 1 B. x = 3, y = 4 C. x = 2, y = 3 D. x = 4, y = 3 Caâu 6:. Than chaùy theo phaûn öùng hoaù hoïc Cacbon + oxi à khí cacbon ñioxit Cho bieát khoái löôïng cuûa cacbon laø 4,5 kg, khoái löôïng cuûa oxi laø 12kg. Khoái löôïng cuûa khí cacbon ñioxit taïo thaønh laø: A. 16,5 kg B. 16,6 kg C. 17 kg D. 14 kg Caâu 7: khi cho hai chaát tham gia phaûn öùng vôùi nhau sau ñoù taïo ra moät chaát môùithì coâng thöùc naøo sau ñaây laø ñuùng khi minh hoaï cho khoái löôïng caùc chaát tröôùc vaø sau phaûn öùng? A m1 + m2 = m3 +m4 B. m1 +m2 = m3 C. m1 - m2 = m3 D . m1 +m2 = m3 - m4 Caâu 8:khi laäp moät phöông trình hoaù hoïc thì ta phaûi tieán haønh theo maáy böôùc cô baûn? A. 1 B. 2 C. 4 D. 3 II. TÖÏ LUAÄN Caâu 9: Phaùt bieåu ñònh luaät baûo toaøn khoái löôïng . Vieát bieåu thöùc theo ñònh luaät Caâu 10: . Cho sô ñoà caùc phaûn öùng hoaù hoïc sau: a. Cu + HCl - - -> CuCl2 + H2 b. Al + O2 ---> ? c. Al + FeSO4 - - -> Al2(SO4)3 + Fe d. C2H2 + O2 - - -> CO2 + H2O Laäp phöông trình hoaù hoïc vaø cho bieát tæ leä soá nguyeân töû, soá phaân töû cuûa caùc chaát trong moãi phaûn öùng Caâu 11:. Cho 130g keõm (Zn) taùc duïng vôùi axit clohidric (HCl) ñöôïc 272g keõm clorua (ZnCl2 ) vaø 4g khí hidro (H2). a. Laäp phöông trình hoaù hoïc cuûa phaûn öùng . b .vieát bieåu thöùc theo ñònh luaät c. Tính khoái löôïng axit clohiric ñaõ tham gia phaûn öùng ---------------------------------------------HEÁT------------------------------------------------------ ÑAÙP ANÙ B.TÖÏ LUAÄN 8ñ Caâu 9(2 Ñ) - Phaùt bieåu ñuùng 1ñ - vieát ñuùng bieåu thöùc 1 ñ Caâu 10: (3 ñ) a). Cu + Cl2 à CuCl2 Tæ leä: soá nguyeân töû Cu : soá phaân töû Cl2 : soá phaân töû CuCl2 = 1 : 1 :1 b). 4Al +3O2 à2AlO3 Tæ leä : 4 : 3 : 2 c) 2Al + 3FeSO4 à Al2(SO4)3 + 3Fe Tæ leä: soá nguyeân töû Al:soá phaân töû FeSO4 :soá phaân töû Al2(SO4)3:soá nguyeân töû Fe = 2: 3:1: 3 Caâu 11: (3ñ ) Laäp ñuùng phöông trình : (1ñ ) Zn + 2HCl à ZnCl2 + H2 Bieåu thöùc ñònh luaät : mZn + mHCl = mZnCl2 + mH2 mHCl = mZnCl2 + mH2 – mZn = 272 + 4 – 130 = 146g (1ñ) -----------------------------HEÁT -------------------------------------- MA TRAÄN NOÄI DUNG MÖÙC ÑOÄ KIEÁN THÖÙC NHAÄN BIEÁT THOÂNG HIEÅU VAÄN DUÏNG TN TL TN TL TN TL SÖÏ BIEÁNÑOÅI CHAÁT C1,2 0,5Ñ PHAÛN ÖÙNG HOAÙ HOÏC C4 0.25Ñ ÑÒNH LUAÄT BAÛO TOAØN KHOÁI LÖÔÏNG C9 2Ñ C7 0,25Ñ C11b 0,5 Ñ PHÖÔNG TRÌNH HOAÙ HOÏC C3,8 0.5Ñ C10 1Ñ C5 0.25Ñ C10,11a 3 Ñ TÍNH TOAÙN C6 0.25Ñ C11c 1,5Ñ TOÅNG 5CAÂU 1,25 Ñ 2CAÂU 3Ñ 2CAÂU 0.5Ñ 3CAÂU 3,5Ñ 1CAÂU 0.25Ñ 1 CAÂU 1,5Ñ Lôùp: Teân: eât’ Kieåm tra: 1 tieát Moân : hoaù 8 ÑEÀ 1 PHAÀN 1: TRAÉC NGHIEÄM Caâu 1: (1 ñieåm) Trong caùc hieän töôïng döôùi ñaây,haõy ghi hieän töôïng hoaù hoïc (HTHH) hoaëc hieän töôïng vaät lí (HTVL) vaøo choã coù caùc daáu chaám, sau moãi cuïm töø moâ taû hieän töôïng sao cho thích hôïp (1ñ) 1. Söï hoaø tan ñöôøng trong nöôùc. (.) 2. Söï phaân huyû cuûa thuoác tím. () 3. Daàu hoaû bò ñoát thaønh khí cacbon ñioxit vaø hôi nöôùc. (.) 4. Söï ngöng tuï cuûa hôi nöôùc. (.) Caâu 2:( 1 ñieåm) Hoaøn thaønh caùc caâu sau ñaây baèng caùch theâm vaøo caùc cuïm töø thích hôïp: phaûn öùng hoaù hoïc, soá löôïng, khoái löôïng, lieân keát (1ñ) Trong dieãn ra söï thay ñoåi giöõa caùc nguyeân töû. Coøncaùc nguyeân töû khoâng thay ñoåi, vì vaäycaùc chaát ñöôïc baûo toaøn. Caâu 3: ( 1 ñieåm) Ngöôøi ta taïo ra voâi soáng baèng caùch nung ñaù voâi. Trong quaù trình nung ñaù voâi coù khí cacbon ñioxit thoaùt ra. Vaäy khi nung, khoái löôïng ñaù voâi seõ bieán ñoåi nhö theá naøo? A. Giaûm ñi. B. Taêng leân. C. Khoâng thay ñoåi. Caâu 4: ( 1ñieåm) Trong caùc phaùt bieåu sau, phaùt bieåu naøo ñuùng, phaùt bieåu naøo sai. Em haõy vieát chöõ Ñ vaøo caâu phaùt bieåu ñuùng, chöõ S vaøo caâu phaùt bieåu sai: a) Khi caùc chaát coù phaûn öùng thì chính laø caùc phaân töû phaûn öùng vôùi nhau. b) Neán loûng chuyeån thaønh hôi laø hieän töôïng hoaù hoïc. c) Khoái löôïng cuûa caùc chaát saûn phaåm baèng khoái löôïng caùc chaát phaûn öùng. d) Trong phaûn öùng hoaù hoïc nguyeân töû khoâng bò phaân chia. PHAÀN 2: TÖÏ LUAÄN Caâu 5: ( 3 ñieåm) Cho sô ñoà caùc phaûn öùng hoaù hoïc sau: 1. Cu + Cl2 - - -> CuCl2 2. Fe2O3 + H2 - - -> Fe + H2O 3. Al + FeSO4 - - -> Al2(SO4)3 + Fe Laäp phöông trình hoaù hoïc vaø cho bieát tæ leä soá nguyeân töû, soá phaân töû cuûa caùc chaát trong moãi phaûn öùng a Caâu 6: (3 ñieåm) Cho 130g keõm (Zn) taùc duïng vöøa ñuû vôùi axit clohidric (HCl) ñöôïc 272g keõm clorua (ZnCl2 ) vaø 4g khí hidro (H2). Laäp phöông trình hoaù hoïc cuûa phaûn öùng . Vieát bieåu thöùc lieân heä veà khoái löôïng giöõa caùc chaát trong phaûn öùng. Tính khoái löôïng axit clohiric ñaõ tham gia phaûn öùng (3ñ) Heát Lôùp: Teân: Teân: Kieåm tra: 1 tieát Moân : hoaù 8 ÑEÀ 2 PHAÀN 1: TRAÉC NGHIEÄM Caâu:1. (1ñieåm) Trong caùc hieän töôïng döôùi ñaây,haõy ghi hieän töôïng hoaù hoïc (HTHH) hoaëc hieän töôïng vaät lí (HTVL) vaøo choã coù caùc daáu chaám, sau moãi cuïm töø moâ taû hieän töôïng sao cho thích hôïp (1ñ) a) Röôïu loaõng ñeå laâu trong khoâng khí bò chua daàn. (.) b) Hoaø tan ñöôøng vaøo nöôùc thaønh nöôùc ñöôøng. (.) c) Daây saét ñeå ngoaøi khoâng khí bò phuû moät lôùp gæ maøu naâu ñoû. (.) d) Thanh ñoàng ñöôïc keùo thaønh caùc sôïi nhoû ñeå laøm da
Tài liệu đính kèm:
 DE_KIEM_TRA_TIET_25.doc
DE_KIEM_TRA_TIET_25.doc





