Đề cương ôn tập Hóa hữu cơ Lớp 9 - Năm học 2016-2017
Bạn đang xem tài liệu "Đề cương ôn tập Hóa hữu cơ Lớp 9 - Năm học 2016-2017", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
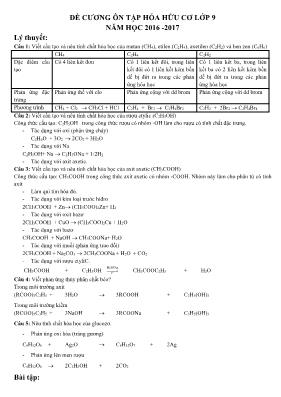
ĐỀ CƯƠNG ễN TẬP HểA HỮU CƠ LỚP 9 NĂM HỌC 2016 -2017 Lý thuyết: Cõu 1: Viết cấu tạo và nờu tớnh chất húa học của metan (CH4), etilen (C2H4), axetilen (C2H2) và ben zen (C6H6) CH4 C2H4 C2H2 Đặc điểm cấu tạo Cú 4 liờn kết đơn Cú 1 liờn kết đụi, trong liờn kết đụi cú 1 liờn kết kộm bền dễ bị đứt ra trong cỏc phản ứng húa học Cú 1 liờn kết ba, trong liờn kết ba cú 2 liờn kết kộm bền dễ bị đứt ra trong cỏc phản ứng húa học Phản ứng đặc trưng Phản ứng thế với clo Phản ứng cộng với dd brom Phản ứng cộng với dd brom Phương trỡnh CH4 + Cl2 CH3Cl + HCl C2H4 + Br2 C2H4Br2 C2H2 + 2Br2 C2H4Br4 Cõu 2: Viết cấu tạo và nờu tớnh chất húa học của rượu etylic (C2H5OH) Cụng thức cấu tạo: C2H5OH trong cụng thức rượu cú nhúm -OH làm cho rượu cú tớnh chất đặc trưng. - Tỏc dụng với oxi (phản ứng chỏy) C2H6O + 3O2 2CO2 + 3H2O - Tỏc dụng với Na C2H5OH+ Na C2H5ONa + 1/2H2 - Tỏc dụng với axit axetic. Cõu 3: Viết cấu tạo và nờu tớnh chất húa học của axit axetic (CH3COOH) Cụng thức cấu tạo: CH3COOH trong cụng thức axit axetic cú nhúm -COOH. Nhúm này làm cho phõn tử cú tớnh axit - Làm quỡ tớm húa đỏ. - Tỏc dụng với kim loại trước hiđro 2CH3COOH + Zn (CH3COO)2Zn+ H2 - Tỏc dụng với oxit bazơ 2CH3COOH + CuO (CH3COO)2Cu + H2O - Tỏc dụng với bazơ CH3COOH + NaOH CH3COONa+ H2O - Tỏc dụng với muối (phản ứng trao đổi) 2CH3COOH + Na2CO3 2CH3COONa + H2O + CO2 - Tỏc dụng với rượu etyliC. CH3COOH + C2H5OH H2SO4đ t0 CH3COOC2H5 + H2O Cõu 4: Viết phản ứng thủy phõn chất bộo? Trong mụi trường axit (RCOO)3C3H5 + 3H2O 3RCOOH + C3H5(OH)3 Trong mụi trường kiềm (RCOO)3C3H5 + 3NaOH 3RCOONa + C3H5(OH)3 Cõu 5: Nờu tớnh chất húa học của glucozơ. - Phản ứng oxi húa (trỏng gương) C6H12O6 + Ag2O C6H12O7 + 2Ag - Phản ứng lờn men rượu C6H12O6 2C2H5OH + 2CO2 Bài tập: Dạng 1: Hoàn thành sơ đồ phản ứng. Bài 1 a. CH4 C2H2 C4H4 C4H6 polibutadien c. CaCO3 ? CaC2 C2H2 ? C2H6 ? PVC d . C H 2 C H 2 C H 3 C H 2 C l C H 3 C H 2 O H e. canxi cacbonat canxi oxit canxi cacbua vinyl clorua PVC vinyl axetilen cloropren cao su cloropren axetilen etan etilen clo etan f. CaCO3 CaO CaC2 C2H2 Bạc axetilua C2H2 etilen PE g. Butan etan etylclorua etan rượu etylic đivinyl butan metan etin benzen h. Điều chế PVC từ đỏ vụi và than đỏ i. Metan axetilen etilen etanol axit axetic natri axetat k. Tinh bột glucozơ ancol etylic andehit axetic. Bài 2: Viết cỏc phương trỡnh phản ứng (ghi rừ điều kiện nếu cú) để thực hiện sơ đồ chuyển hoỏ sau: a) CH2 = CH2 (1) C2H5OH (2) CH3COOH (3) (CH3COO)2Zn CH3COOC2H5 (5)CH3COONa b) CaCO3 (1) CaO 0C(2)2000 C CaC2 2H O(3) C2H2 20H ,Pdt (4) C2H4 (5) C2H5OH (6) CH3COOH (7) CH3COONa c) Tinh bột (1) Glucozơ (2) Rượu etylic (3) Axit axetic Bài 3: Hoàn thành �R� ph�ơng t괈٨nh: 1/ C + H2 oCNi 500, ............; 2/ CH3COONa + NaOH toCaO, .......... + .......... 3/ Al4C3 + H2O .......... + ..........; 4/ CH4 + O2 to ............ + ............ 5/ CH4 + Cl2 ỏnhsỏng CH3Cl + .......... ; 6/ .......... + Cl2 ỏnhsỏng CH2Cl2 + ............ 7/ CH2Cl2 + ....... ỏnhsỏng CHCl3 + ........; 8/ CHCl3 + Cl2 ỏnhsỏng .......... + .......... 9/ C2H4 + H2 toNi, ........... ; 10/ n (CH2 = CH2) xtPto ,, ............. (PE) 11/ C2H4 + Br2 OH 2 ...........; 12/ C2H5OH oCđSOH 170,42 .......... + ........... 13/ C2H2 + H2 toPd , .......... ; 14/ C2H2 + H2 toNi, ........... 15/ CaC2 + H2O .......... + ..........; 16/ CH4 ln,1500 loC .......... + ........... 17/ C2H2 + Br2 OH 2 ............ ; 18/ C2H2 + HCl 2HgCl ............ 19/ C2H2 + O2 to ............ + ............; 20/ C2H2 oCChoattớnh 600, ............ 21/ C6H6 + Br2 lỏng toFe, ........... + .......... ; 22/ C6H6 + H2 toNi, .............. 23/ C6H6 + Cl2 ỏnhsỏng ..............; 24/ C6H6 + HNO3 đSOH 42 ............. + .............. 25/ C6H6 + O2 to ........... + .............; 26/ C6H12O6 oCmenruou 3230, ........... + ............ 27/ C2H4 + H2O toloóngSOH ,42 .............; 28/ C2H5OH + Na .............. + ........... 29/ C2H5OH + K .............. + ...........; 30/ C2H5OH + O2 to ............ + ............ (4) 31/ C2H5OH + O2 mengiam ........... + ..........; 32/ C4H10 + O2 xỳctỏcto, ............. + ............ 33/ CH3COOH + Mg .............. + ........; 34/ CH3COOH + NaOH ............... + ........... 35/ CH3COOH + Na2CO3 ........+ ...... + .....; 36/ CH3COOH + ZnO ................ + ........... 37/ CH3COONa + H2SO4 ............ + ........; 38/ (CH3COO)2Ba + K2SO4 ............... + ......... 39/ CH3COOH + C2H5OH tođSOH ,42 .............+ ................ 40/ CH3COOC2H5 + NaOH ........ + ........; 41/ C6H12O6 + Ag2O toNH ,3 .............. + ....... 42/ CH3COOH + O2 to ........... + ...........; 43/ C6H12O6 + O2 to ........... + ........... Dạng 2: Nhận biết, phõn biệt �R� hợp �hất hữu �ơ. Bài 1. Dựng phương phỏp húa học phõn biệt cỏc khớ khụng màu sau: a. CH4, CO2, C2H4, C2H2 Dựng Ca(OH)2 - CO2 phản ứng tạo kết tủa trắng. CO2 + Ca(OH)2 CaCO3 + H2O - Cũn lại ba khớ CH4 và C2H4, C2H2 Dựng dung dịch AgNO3/NH3 - C2H2 phản ứng tạo kết tủa vàng. C2H2 + 2AgNO3 + 2NH3 C2Ag2 + 2NH4NO3 - Cũn lại hai khớ CH4 và C2H4 Dựng dung dịch nước brom - C2H4 phản ứng làm mất màu nước brom C2H4 + Br2 C2H4Br2 - Cũn lại là khớ CH4 b. C3H4, SO2, C2H4, C2H6 Dựng Ca(OH)2 - CO2 phản ứng tạo kết tủa trắng. SO2 + Ca(OH)2 CaSO3 + H2O - Cũn lại ba khớ C3H4 và C2H4, C2H6 Dựng dung dịch AgNO3/NH3 - C3H4 phản ứng tạo kết tủa vàng. C3H4 + AgNO3+ NH3 C3H3Ag + NH4NO3 - Cũn lại hai khớ C2H4 và C2H6 Dựng dung dịch nước brom - C2H4 phản ứng làm mất màu nước brom C2H4 + Br2 C2H4Br2 - Cũn lại là khớ C2H6 c. CH4, O2, C2H4, C2H2 (HS tự giải) d. H2, CO2, C2H4, SO2 (HS tự giải) Bài 2. Dựng phương phỏp húa học phõn biệt cỏc chất sau: a. C6H6, C2H5OH, CH3COOH (benzen, rượu etylic, axit axetic) Dựng quỡ tớm - CH3COOH làm quỡ tớm húa đỏ. - Cũn lại 2 chất là C6H6, C2H5OH Dựng Na - C2H5OH phản ứng cú khớ bay ra C2H5OH + Na C2H5ONa + 1/2H2 - Cũn lại là C6H6 b. CH3COOH, C6H12O6, C12H22O11 ( Axit axetic, glucozơ, saccarozơ) Dựng quỡ tớm - CH3COOH làm quỡ tớm húa đỏ. - Cũn lại 2 chất là C6H12O6, C12H22O11 Dựng dung dịch AgNO3/NH3 - C6H12O6 phản ứng tạo kết tủa trắng. C6H12O6 + Ag2O C6H12O7 + 2Ag - Cũn lại là C12H22O11 c. Glucozơ, xenlulozơ, tinh boọt. Dựng dung dịch AgNO3/NH3 - Glucozơ (C6H12O6 ) phản ứng tạo kết tủa trắng. C6H12O6 + Ag2O C6H12O7 + 2Ag - Cũn lại là tinh bột và xenlulozơ Dựng dung dịch iot. - Chất nào tạo màu xanh đặc trưng là tinh bột - Chất cũn lại là xenlulozơ Dạng 3: XR� định �ụng thứ� phõn tử hợp �hất hữu �ơ theo �ụng thứ� đơn giản nhất 5. Khi đốt chỏy hoàn toàn 2,2g hợp chất hữu cơ A thu được 4,4g CO2 và 1,8g H2O. Ngoài ra khụng cú chất nào khỏc. Biết rằng 0,84 lớt hơi hợp chất A (đktc) cú khối lượng là 3,3g; tỡm CTHH của hợp chất A? 6. a. Xỏc định CT đơn giản của chất A chứa 80%C và 20%H. b. xỏc định CTPT của A chứa 85,71%C và 14,29%H biết 1 lớt khớ A ở đktc nặng 1,25g? 7. Một hợp chất hữu cơ cú khối lượng mol là 60g, trong đú C chiếm 40%, H chiếm 6,66% cún lại là O. Tớm CTPT của h/c? 8. Đốt chỏy hoàn toàn 2,3g một hchc A người ta thu được 2,24 lớt CO2 ở đktc và 2,7g nước.Xỏc định CTPT của chất A, biết A cú phõn tử khối là 46. 9. Hợp chất A cú thành phấn cỏc nguyờn tố: 53,33%C; 15,55%H; 31,12%N. Tỡm CTPT của A, biết A cú phõn tử khối là 46? 10. Hợp chất hữu cơ A cú tỉ khối đối với H2 bằng 13. Đốt chỏy A người ta thu được khớ CO2 và hơi nước. 11. Hợp chất hữu cơ B cú khối lượng mol phõn tử bằng 72. Thành phần phõn tử gồm cú 83,34%C và 16,66%H? 12. Đốt chỏy hoàn toàn 0,45g một hợp chất hữu cơ X, thu được 0,66g CO2 và 0,27g H2O. Biết X cú tỉ khối đối với Hidro là 15. a. Tớnh thành phần % theo khối lượng cỏc nguyờn tố của hchc X? b. Tỡm CTPT của hchc X? 13. Xỏc định CTPT của hidrocacbon biết rằng chất đú chứa 75%C; 25%H. Biết tỉ khối của nú so với oxi bằng 0,5? 14. Khi đốt chỏy hoan toàn 1,32g chất hữu cơ A thỡ thu được 3,96g khớ CO2 và 0,72g H2O. a. Tớnh thành phần % về khối lượng cỏc nguyờn tố cú trong phõn tử A? b. Lập CT đơn giản của A? 15. Viết CTCT của cỏc hchc sau: C3H6; C4H8; C4H10; C3H7Cl; C3H8O? 16. Một hchc A cú hai nguyờn tố C và H. Đốt chỏy 4,5g chất hữu cơ A thu được 8,1g nước. a. Viết CT đơn giản của A? b. Cho biết k.l mol của A bằng 30, Hóy xỏc định A? c. Tớnh thành phần % cỏc nguyờn tố cấu tạo nờn A? 17. Đốt chỏy hoàn toàn m gam hchc X cần dựng 28,8g oxi, thu được 39,6g CO2 và 20,16 lớt hơi nước (đktc). a. xỏc định CT đơn giản của X? b. Xỏc định CTPT của X biết X cú tỉ khối đối với khụng khớ : 5.86 < d< 6,55. c. Tớnh m? 18. Cho hh X gồm 70% CH4 và 30% C2H6 theo thể tớch. a. Tớnh thể tớch kk cần dựng để đốt chỏy 33,6 lớt hh X? b. Tớnh k.l cỏc chất tạo thành? c. Tớnh tỉ khối của X đối với kk? 19. Đốt chỏy hoàn toàn 6,2g một hc A (gồm C, H, N) thu được 17,6g CO2 và 4,2g H2O. Trong đktc, khối lượng của 1 lớt hơi chất A là 4,15g. Hóy tỡm CTPT của A? 20. Để đốt chỏy 0,55g một hchc A (gồm C, H, O) cần 1,05 lớt O2 thu được 0,7 lớt CO2 và 3,3g nước. Xỏc định CTHH của hc A? (cỏc thể tớch khớ đo ở đktc) 21. Đốt chỏy 1,5g chất hữu cơ thu được 1,76g khớ CO2; 0,9g nước và 0,448 lớt khớ NH3. Nếu húa hơi 1,5g chất hữu cơ A thỡ thu được 0,448 lớt khớ. Xỏc định CTPT của hchc A? (cỏc thể tớch khớ đo ở đktc) Bài 1: Hợp chất X cú % khối lượng cacbon, hidro và oxi lần lượt bằng 81,08%,8,1% và cũn lại là oxi. Tỡm CTPT của X biết MX = 148g/mol Bài 2: Hợp chất X cú % khối lượng cacbon, hidro lần lượt là: 88,235%, 11,765%, biết tỉ khối của X so với khụng khớ gần bằng 4,69. Tỡm CTPT của X Bài 3: Đốt chỏy hoàn toàn 0,3 gam chất A ( phõn tử chỉ chứa C,H,O) thu được 0,44 gam khớ CO2 và 0,18 g H2O. Thể tớch hơi của 0,3 g chất A bằng thể tớch của 0,16 g khớ O2 ( ở cựng điều kiện về nhiệt độ, ỏp suất). Xỏc định CTPT của A Bài 4: Đốt chỏy hoàn toàn 2,2 g chất hữu cơ A, được 4,4 g CO2 và 1,8 g H2O 1. Xỏc định CTĐGN của chất A 2. Xỏc định CTPT chất A biết rằng nếu làm bay hơi 1,1 g chất A thỡ thể tớch hơi thu được đỳng bằng thể tớch của 0,4 g khớ O2 ở cựng nhiệt độ và ỏp suất. Bài 5: Đốt chỏy hoàn toàn 4,1 g chất hữu cơ A được 2,65 g Na2CO3, 1,35 g H2O và 1,68 lớt CO2 (đktc). Xỏc định CTĐGN của chất A Bài 6: Tỡm CTPT của mỗi chất trong từng trường hợp sau: a. Đốt chỏy 0,6g chất hữu cơ A thỡ thu được 0,88g CO2 và 0,36g H2O và 2A/H d = 30 b. Đốt chỏy 7g chất hữu cơ B thỡ thu được 11,2 lớt CO2 (đkc) và 9g H2O. Khối lượng riờng của B ở đkc là 1,25g/l c. Đốt chỏy hoàn toàn 10g chất hữu cơ C thu được 33,85g CO2 và 6,94g H2O. Tỷ khối hơi của C so với khụng khớ là 2,69. ĐS: C2H4O2; C2H4; C6H6 Bài 7: Đốt chỏy hoàn toàn m(g) một Hydrocacbon A thỡ thu được 2,24 lớt CO2 (đkc) và 3,6g H2O. a. Tớnh m và % khối lượng cỏc nguyờn tố trong A ? b. Xỏc định CTN; CTPT của A biết 2A/H d = 8 ĐS: 1,6g; 75%; 25%; CH4 Bài 8: Đốt chỏy hoàn toàn 0,9g một chất hữu cơ cú thành phần gồm cỏc nguyờn tố C, H, O người ta thu được 1,32g CO2 và 0,54g H2O. Khối lượng phõn tử chất đú là 180đvC. Hóy xỏc định CTPT của chất hữu cơ núi trờn ? ĐS: C6H12O6 Bài 9: Đốt chỏy hoàn toàn 5,2g hợp chất hữu cơ A rồi cho sản phẩm lần lượt qua bỡnh H2SO4 đđ thỡ khối lượng bỡnh tăng 1,8g và qua bỡnh đựng nước vụi trong dư thỡ cú 15g kết tủa. Xỏc định CTPT của A biết 2A/O d = 3,25 ĐS: C3H4O4 Bài 10: Đốt chỏy hoàn toàn một lượng Hydrocacbon A rồi cho toàn bộ sản phẩm lần lượt qua bỡnh một đựng H2SO4 đđ rồi qua bỡnh hai đựng nước vụi trong dư. Sau thớ nghiệm khối lượng bỡnh một tăng 0,36g và bỡnh hai cú 2g kết tủa trắng. a. Tớnh % khối lượng cỏc nguyờn tố trong A ? b. Xỏc định CTN và CTPT của A biết dA/KK = 0,965 ? c. Nếu ta thay đổi thứ tự hai bỡnh trờn thỡ độ tăng khối lượng mỗi bỡnh ra sao sau thớ nghiệm? ĐS: 85,71%; 14,29%; C2H4; tăng 1,24g và khụng đổi Dạng 4: XR� định �ụng thứ� phõn tử dựa vào phản ứng Bài 11: Đốt chỏy hoàn toàn 100ml hơi chất (A) cần 250ml Oxy tạo ra 200ml CO2 và 200ml hơi nước. Tỡm CTPT của (A) biết rằng cỏc thể tớch đo trong cựng điều kiện nhiệt độ, ỏp suất ?ĐS: C2H4O Bài 12: Trộn 10ml Hydrocacbon A với 60ml O2 (dư) rồi đốt. Sau phản ứng làm lạnh thu được 40ml hỗn hợp khớ, tiếp tục cho hỗn hợp khớ qua nước vụi trong dư thỡ cũn 10ml khớ. Tỡm CTPT của A ? Biết rằng tất cả cỏc thể tớch đo trong cựng điều kiện nhiệt độ, ỏp suất. ĐS: C8H12 Bài 13: Đốt 200cm3 hơi một chất hữu cơ chứa C; H; O trong 900cm3 O2 (dư). Thể tớch sau phản ứng là 1,3 lớt sau đú cho nước ngưng tụ cũn 700cm3 và sau khi cho qua dung dịch KOH cũn 100cm3. Xỏc định CTPT của chất hữu cơ ? Biết rằng cỏc khớ đo trong cựng điều kiện nhiệt độ, ỏp suất. ĐS: C3H6O Bài 14: Chất hữu cơ X ở thể khớ, khi đốt 1 lớt khớ X cần đỳng 5 lớt khớ oxi. Sau pư thu được 3 lớt khớ CO2 và 4 lớt hơi nước. Xỏc định CTPT của A. biết thể tớch cỏc khớ đo ở cựng điều kiện nhiệt độ và ỏp suất. ĐS:C3H8 Bài 15:Đốt chỏy hoàn toàn 0,01 mol hợp chất hữu cơ X bằng 0,616 lớt O2 (vừa đủ) thu được 1,344 lớt hỗn hợp gồm CO2, N2 và hơi nước. Sau khi ngưng tụ hơi nước, hỗn hợp cũn lại cú thể tớch là 0,56 lớt và cú tỉ khối so với hidro bằng 20,4. Thể tớch cỏc khớ đo ở đktc. Xỏc định CTPT của X.. ĐS: C2H7N Bài 16: Đốt chỏy hoàn toàn 0,1 mol hợp chất hữu cơ (D) cần vừa đủ 14,4 gam oxi, thấy sinh ra 13,2 gam CO2 và 7,2 gam nước. a. Tỡm phõn tử khối cuả (D). b. Xỏc định cụng thức phõn tử của (D). ĐS: 60, C3H8O Bài 17: Đốt chỏy hoàn toàn 112 cm3 một hydrocacbon (A) là chất khớ ở (đktc) rồi dẫn sản phẩm lần lượt qua bỡnh (I) đựng H2SO4 đậm đặc và bỡnh (II) chứa KOH dư người ta thấy khối lượng bỡnh (I) tăng 0,18 gam và khối lượng bỡnh (II) tăng 0,44 gam.Xỏc định CTPT (A). ĐS: C2H2 Dạng 5: Tớnh toRn theo ph�ơng t괈٨nh húa họ� Hid괈o�a�bon + Oxi Bài 18: Đốt chỏy hoàn toàn 11,2 gam C2H4 trong khụng khớ a. Viết phương trỡnh phản ứng. b. Tớnh khối lượng cỏc sản phẩm thu được c. Tớnh thể tớch khụng khớ cần dựng(đktc) biết oxi chiếm 1/5 thể tớch khụng khớ. ĐS: 35,2g; 14,4g; 134,4 (l) Bài 19: Đốt chỏy hoàn toàn 6,72 lit CH4 trong khụng khớ a. Viết phương trỡnh phản ứng. b. Tớnh khối lượng cỏc sản phẩm thu được c. Tớnh thể tớch khụng khớ cần dựng(đktc) biết oxi chiếm 1/5 thể tớch khụng khớ. ĐS: 13,2g; 10,8g; 67,2 (l) Bài 20: Đốt chỏy hoàn toàn 13,44 lit C2H2 trong khụng khớ a. Viết phương trỡnh phản ứng. b. Tớnh khối lượng cỏc sản phẩm thu được c. Tớnh thể tớch khụng khớ cần dựng(đktc) biết oxi chiếm 1/5 thể tớch khụng khớ. ĐS: 52,8g; 10,8g; 168 (l) Bài 21: Đốt chỏy hoàn toàn 22,4 lit hỗn hợp gồm CH4 và H2 thu được 32,4 g H2O a. Viết phương trỡnh phản ứng. b. Tớnh thể tớch khụng khớ cần dựng(đktc) biết oxi chiếm 1/5 thể tớch khụng khớ. ĐS: 180,4 (l) Hid괈o�a�bon + dd b괈om Bài 22: Cho 1,12 lớt khớ axetilen (C2H2) tỏc dụng với dung dịch brom 8% thu được C2H2Br4. a. Viết PTHH b. Tớnh khối lượng sản phẩm thu được. c. Tớnh khối lượng dung dịch brom cần dựng. ĐS: 17,3g; 200g Bài 23: Cho 2,24 lớt khớ Etilen (C2H4) tỏc dụng với dung dịch brom 20% . a. Viết PTHH b. Tớnh khối lượng sản phẩm thu được. c. Tớnh khối lượng dung dịch brom cần dựng. ĐS: 18,8g; 800g Bài 24: Cho 1,3 gam khớ axetilen (C2H2) tỏc dụng với dung dịch brom 25% thu được C2H2Br4. a. Viết PTHH b. Tớnh khối lượng sản phẩm thu được. c. Tớnh khối lượng dung dịch brom cần dựng. ĐS: 17,3g; 64g Bài 25: Cho 2,8 gam khớ Etilen (C2H4) tỏc dụng với dung dịch brom 5% . a. Viết PTHH b. Tớnh khối lượng sản phẩm thu được. c. Tớnh khối lượng dung dịch brom cần dựng. ĐS: 18,8g; 320g Dạng 6: Bài tập hỗn hợp Hỗn hợp hid괈o�a�bon + oxi Bài 26: Đốt chỏy 22,4 dm3 hỗn hợp etan(C2H6 ) và axetilen(C2H2) thu được 40,34 dm3 H2O a. Tớnh số mol etan và axetin cú trong 22,4 dm3 hỗn hợp b. Tớnh số gam Oxi cần thiết để đốt chỏy hoàn toàn 22,4 dm3 hỗn hợp đú c. Tớnh tỉ khối hơi của hỗn hợp khớ đú đối với khụng khớ. Cỏc thể tớch khớ đo ở đktc ĐS: 0,4; 0,6; 92,8g; 0,95 Bài 27: Đốt chỏy 11,2 lớt hỗn hợp gồm CH4 và H2(ở đktc) thu được 16,2 g H2O. a. Viết cỏc phương trỡnh phản ứng. b. Tớnh % (V) mỗi khớ trong hỗn hợp. �. Tớnh thể tớch oxi cần dựng. ĐS: 0,4; 0,1; 80%;20%; 19,04 lit Bài 28: Đốt chỏy hoàn toàn 8,4 lớt hỗn hợp khớ CO, CH4 cần dựng 6,72 lit khớ O2. a. Viết cỏc phương trỡnh phản ứng. b. Tớnh % theo thể tớch và theo khỗi lượng của mỗi khớ trong hỗn hợp. ĐS: 80%; 20%; 87,5%; 12,5% Bài 29: Đốt chỏy hoàn toàn 54 gam hỗn hợp khớ C2H6, C3H6 trong oxi dư thu được 84 lit khớ CO2. a. Viết cỏc phương trỡnh phản ứng. b. Tớnh % theo thể tớch và theo khỗi lượng của mỗi khớ trong hỗn hợp. ĐS: 50%; 50%; 41,7%; 58,3% Bài 30: Đốt chỏy hoàn toàn 5,3 gam hỗn hợp khớ C2H2, CH4 trong oxi dư thu được 7,84 lit khớ CO2. a. Viết cỏc phương trỡnh phản ứng. b. Tớnh % theo thể tớch và theo khỗi lượng của mỗi khớ trong hỗn hợp. ĐS: 16,7%; 83,3%; 24,5%; 75,5% Bài 31: Đốt chỏy hoàn toàn 28 ml hỗn hợp khớ C2H2, CH4 cần dựng 67,2 ml khớ O2. a. Viết cỏc phương trỡnh phản ứng. b. Tớnh % theo thể tớch của mỗi khớ trong hỗn hợp. ĐS: 80%; 20% Bài 32: Đốt chỏy hoàn toàn 10,6 gam hỗn hợp khớ C2H2, C3H4 trong oxi. Đem toàn bộ sản phẩm qua dung dịch Ca(OH)2 dư thu được 80g kết tủa. a. Viết cỏc phương trỡnh phản ứng. b. Tớnh khỗi lượng của mỗi khớ trong hỗn hợp. ĐS: 2,6g; 8g Bài 33: Đốt chỏy hoàn toàn 14,56 lit hỗn hợp khớ C2H2, CH4 trong oxi. Đem toàn bộ sản phẩm qua dung dịch H2SO4 đ thấy khối lượng bỡnh tăng lờn 18,9g. a. Viết cỏc phương trỡnh phản ứng. b. Tớnh % theo thể tớch của mỗi khớ trong hỗn hợp. ĐS: 38,5%; 61,5% Hỗn hợp hid괈o�a�bon + dd b괈om Bài 34: Cho 5,6 lit (đktc) CH4 và C2H2 đi qua nước brom dư thấy cú 4 g brom tham gia phản ứng. a. Tớnh thể tớch mỗi khớ trong hỗn hợp. b. Tớnh % theo thể tớch của mỗi khớ trong hỗn hợp. ĐS: 5,32 lit; 0,28 lit; 95%; 5% Bài 35; Cho 6,72 lit (đktc) CH4 và C2H4 đi qua nước brom dư thấy 16 g brom tham gia phản ứng a. Tớnh thể tớch mỗi khớ trong hỗn hợp. b. Tớnh % theo thể tớch của mỗi khớ trong hỗn hợp. ĐS: 4,48 lit; 2,24 lit; 66,7%; 33,3% Bài 36: Cho 5,6 lit (đktc) C2H4 và C2H2 đi qua nước brom dư thấy cú 56 g brom tham gia phản ứng. a. Tớnh thể tớch mỗi khớ trong hỗn hợp. b. Tớnh % theo thể tớch của mỗi khớ trong hỗn hợp. ĐS: 3,36 lit; 2,24 lit; 60%; 40% Bài tập liờn quan đến % khớ t괈ong khớ thiờn nhiờn. Bài 37: Đốt chỏy V (l) khớ thiờn nhiờn chứa 96% CH4, 2% N2 và 2% CO2 về thể tớch. Toàn bộ sản phẩm chỏy được dẫn qua dung dịch Ca(OH)2 dư thấy tạo ra 4,9 g kết tủa. a. Viết phương trỡnh húa học( biết N2 khụng chỏy) b. Tớnh V. ĐS:1,12 lit Bài 38: Đốt chỏy V (l) khớ thiờn nhiờn chứa 95% CH4, 2% N2 và 3% CO2 về thể tớch. Toàn bộ sản phẩm chỏy được dẫn qua dung dịch Ca(OH)2 dư thấy tạo ra 10 g kết tủa. a. Viết phương trỡnh húa học( biết N2 khụng chỏy) b. Tớnh V. ĐS:2,286 lit Dạng 7: bài tập liờn quan đến 괈�ợu DD R�ợu tR� dụng với Na → Tớnh thể tớ�h khớ H2 Bài 39: Cho kim loại Na tỏc dụng với 10ml rượu etylic 960. a. Tỡm thể tớch và k.l rượu etylic đó tham gia pư? b. Tớnh Vhidro thu được ở đktc. (Biết dr = 0,8g/ml; dnước = 1g/ml) ĐS: 9,6 ml; 7,68g; 2,12 lit Bài 40: Cho kim loại Na tỏc dụng với 40ml rượu etylic 920. a. Viết Phương trỡnh húa học b. Tớnh Vhidro thu được ở đktc. (Biết dr = 0,8g/ml; dnước = 1g/ml) ĐS: 9,16 lit Bài 41: Cho kim loại Na tỏc dụng với 20g rượu etylic 920. a. Tỡm thể tớch và k.l rượu etylic đó tham gia pư? b. Tớnh Vhidro thu được ở đktc. (Biết dr = 0,8g/ml; dnước = 1g/ml) ĐS: 23 ml; 18,4g; 5,6 lit Bài 42: Cho 25ml rượu etylic 900 tỏc dụng với kim loại K dư. a. Tớnh thể tớch và k.l rượu etylic đó tham gia pư? b. Tớnh Vhidro thu được ở đktc. (Biết dr = 0,8g/ml; dnước = 1g/ml) ĐS: 22,5 ml; 18g; 5,9 lit DD R�ợu tR� dụng với Na biết thể tớ�h khớ H2 tớnh độ 괈�ợu Bài 43: Cho 87g dd rượu etylic chưa rừ độ rượu, tỏc dụng với Na lấy dư thỡ thu được 28 lớt H2 (đktc). a. Tớnh k.l của rượu etylic
Tài liệu đính kèm:
 de_cuong_on_tap_hoa_huu_co_lop_9_nam_hoc_2016_2017.pdf
de_cuong_on_tap_hoa_huu_co_lop_9_nam_hoc_2016_2017.pdf






